doi: 10.56294/hl2023263
REVISIÓN
Impact of Oral Contraceptives on Periodontal Health: Influence of Steroid Hormones
Impacto de los Anticonceptivos Orales en la Salud Periodontal: Influencia de las Hormonas Esteroideas
Edward Alejandro Hansen1
1Universidad Abierta Interamericana, Facultad de Medicina y Ciencias de la Salud, Carrera de Odontologia. Buenos Aires, Argentina.
Citar como: Hansen EA. Impact of Oral Contraceptives on Periodontal Health: Influence of Steroid Hormones. Health Leadership and Quality of Life. 2023; 2:263. https://doi.org/10.56294/hl2023263
Enviado: 03-05-2023 Revisado: 18-07-2023 Aceptado: 14-10-2023 Publicado: 15-10-2023
Editor: PhD.
Prof. Neela Satheesh ![]()
ABSTRACT
Introduction: the oral cavity constitutes a dynamic niche susceptible to environmental and physiological changes. Alterations in its microbiome can lead to pathologies such as caries and periodontal disease, the latter being one of the main causes of tooth loss worldwide. Candida albicans has been identified as the most prevalent fungus in the oral microbiota, although detections of non-albicans species have increased in the last decade. In addition, steroid hormones such as estrogens and progesterone, present in oral contraceptives, have been shown to modulate the periodontal inflammatory response, exacerbating conditions such as gingivitis and favoring the progression of periodontal disease.
Development: this work explored the impact of oral contraceptives and steroid hormones on bacterial plaque-induced gingivitis and periodontitis progression. The most recent classifications of periodontal disease, which group pathologies according to stages and grades, were addressed, allowing a better assessment of hormonal factors in their evolution. The findings supported the relationship between oral contraceptive use and increased susceptibility to gingival inflammation, especially in advanced clinical conditions.
Conclusions: steroid hormones, present in contraceptives, played an important role in modulating the oral microbiome and periodontal inflammation. Although no direct relationship was found in mild cases, in advanced stages of periodontal disease the hormonal impact was significant. These results highlight the need to monitor hormonal factors in dental treatment and to promote personalized preventive strategies.
Keywords: Periodontal Disease; Gingivitis; Oral Microbiome; Oral Contraceptives; Steroid Hormones.
RESUMEN
Introducción: la cavidad bucal constituye un nicho dinámico susceptible a cambios ambientales y fisiológicos. Alteraciones en su microbioma pueden llevar a patologías como caries y enfermedad periodontal, esta última siendo una de las principales causas de pérdida dentaria a nivel mundial. Se ha identificado a Candida albicans como el hongo más prevalente en la microbiota bucal, aunque en la última década han aumentado las detecciones de especies no albicans. Además, hormonas esteroideas como los estrógenos y la progesterona, presentes en anticonceptivos orales, han demostrado modular la respuesta inflamatoria periodontal, exacerbando condiciones como la gingivitis y favoreciendo la progresión de la enfermedad periodontal.
Desarrollo: este trabajo exploró el impacto de los anticonceptivos orales y las hormonas esteroideas en la gingivitis inducida por placa bacteriana y en la progresión de la periodontitis. Se abordaron las clasificaciones más recientes de la enfermedad periodontal, que agrupan las patologías según estadios y grados, permitiendo una mejor evaluación de los factores hormonales en su evolución. Los hallazgos respaldaron la relación entre el uso de anticonceptivos orales y una mayor susceptibilidad a la inflamación gingival, especialmente en condiciones clínicas avanzadas.
Conclusiones: las hormonas esteroideas, presentes en los anticonceptivos, desempeñaron un papel importante en la modulación del microbioma bucal y la inflamación periodontal. Aunque no se encontró una relación directa en casos leves, en estadios avanzados de enfermedad periodontal el impacto hormonal fue significativo. Estos resultados destacan la necesidad de monitorear factores hormonales en los tratamientos odontológicos y fomentar estrategias preventivas personalizadas.
Palabras clave: Enfermedad Periodontal; Gingivitis; Microbioma Bucal; Anticonceptivos Orales; Hormonas Esteroideas.
INTRODUCCIÓN
La cavidad bucal es una puerta de entrada del cuerpo humano y está en frecuente contacto con el ambiente externo, ante lo cual, las comunidades microbianas que la colonizan están expuestas a cambios según las condiciones ambientales,(1) y alteraciones en el equilibrio ecológico de este nicho pueden conducir a patologías como caries dental y enfermedad periodontal.(2) Según un análisis sistemático publicado en Lancet 2017, la enfermedad periodontal fue la décimo primera patología humana más prevalente afectando a 750,8 millones de personas en el mundo entero (GBD 2017) y siendo una de las mayores causas de pérdida dentaria, hecho que compromete a la masticación, la estética y la calidad de vida de los pacientes afectados. Publicaciones que datan del año 2005 sugieren que los organismos residentes del microbioma bucal y su genoma son componentes críticos de la salud y la enfermedad.(3,4) En el 2010 se publicó el primer trabajo que determinó el componente fúngico de la microbiota bucal humana en condiciones de salud, basados en análisis de la región ITS (espaciador transcripcional interno fúngico). El estudio concluyó que, en las condiciones estudiadas, la cavidad bucal estaría colonizada por más de 70 géneros fúngicos, siendo el género Candida el más prevalente, aislándose en el 75 % de los participantes. Este dato coincide con el consenso global, el cual establece que, en promedio, el 40-50 % de la población saludable es portadora del género Candida en saliva, mucosa bucal y biofilm subgingival;(5,6,7) existiendo condiciones locales y sistémicas que pueden transformar este nicho ecológico en un sitio favorable para el sobrecrecimiento de levaduras pertenecientes a este género,(8) siendo C. albicans la especie más aislada. Sin embargo, en los últimos diez años, algunos estudios han determinado un aumento en la frecuencia de recuperación de especies de Candida no Candida albicans (NAC).(9,10,11) Además, la respuesta inmunológica del hospedero frente al desafío impuesto por los microorganismos de la biopelícula puede ser modulada tanto por factores locales como sistémicos. Entre los factores locales y/o sistémicos que se han asociado con este desplazamiento en la distribución bucal de especies de Candida, se han descripto, la portación de dispositivos protéticos,(12) la edad avanzada,(13) pacientes oncológicos sometidos a quimioterapia y radioterapia,(14,15,16) diabéticos con pobre control metabólico,(17) varones que consumen esteroides androgénicos,(18) y mujeres que usan anticonceptivos bucales.(19,20) Varios estudios indican una correlación positiva en la incidencia de enfermedad gingival con las concentraciones de hormonas sexuales, aumentadas durante la pubertad, el ciclo menstrual y el embarazo, modulando en particular el proceso inflamatorio que se genera como respuesta a la noxa microbiana.(21,22,23,24,25,26,27,28,29,30) Los estrógenos son moléculas lipofílicas, los cuales en su forma natural están la estrona, el 17 β estradiol y estriol. El estradiol es el estrógeno más potente y es secretado por los ovarios, testículos, placenta, así como también por los tejidos periféricos. Sufre biotransformación hepática rápida en la cual es convertida por 17b- hidroxiesteroide deshidrogenasa a estrona, que luego se convierte en 16a-hidroxilación y 17-ceto y se reduce a estriol, que es el principal metabolito urinario. El etinilestradiol es el estrógeno semi-sintético más utilizado en anticonceptivos orales. Esta variación facilita el crecimiento de microorganismos patógenos asociados a la inflamación gingival y a la enfermedad periodontal (EP). El aumento de la progesterona durante el tercer trimestre del embarazo coincide con la presencia de EP, y el nivel de progesterona durante el embarazo se correlacionó positivamente con la cantidad de sangrado periodontal. Las infecciones de diverso origen que se producen durante el embarazo pueden poner en riesgo el normal desarrollo de éste, e incluso afectar de manera negativa a la salud del feto. A este respecto las patologías que con más frecuencia se observan en asociación con la presencia de procesos infecciosos son el parto pretérmino y el bajo peso al nacer.(31,32,33,34,35,36,37)
Objetivo
Analizar la influencia de los anticonceptivos orales y las hormonas esteroideas en la modulación de la gingivitis inducida por placa bacteriana y su relación con la progresión de la enfermedad periodontal, considerando su impacto en la salud bucal y sistémica de las mujeres en diferentes etapas hormonales.
DESARROLLO
En 2017 la Academia Americana de Periodoncia (AAP) y la Federación Europea de Periodoncia (EFP) han elaborado un nuevo sistema de clasificación de las patologías y alteraciones periodontales y periimplantarias.
Según lo publicado por la Sociedad Española de Periodoncia y Osteointegración (2017): “…por primera vez, se clasifican las patologías y alteraciones periimplantarias conjuntamente con las patologías y alteraciones periodontales. Ahora, la periodontitis se caracteriza por medio de dos dimensiones, estadios y grados.”
Con el objetivo de poder especificar y definir con mayor exactitud la enfermedad periodontal, se consideró:
1) Salud periodontal y patologías/condiciones gingivales.
2) Periodontitis.
3) Trastornos del desarrollo y adquiridos y manifestaciones periodontales de enfermedades sistémicas.
4) Patologías y condiciones periodontales.
Los objetivos en este trabajo están vinculados en particular al punto Gingivitis inducida por placa bacteriana donde el consumo de los anticonceptivos se lo incluye dentro de factores que modifican la gingivitis inducida por biofilm, exacerbada por hormonas esteroideas (Punto 2, B, i), e) - anticonceptivos orales -) de la nueva clasificación, según la figura 1.
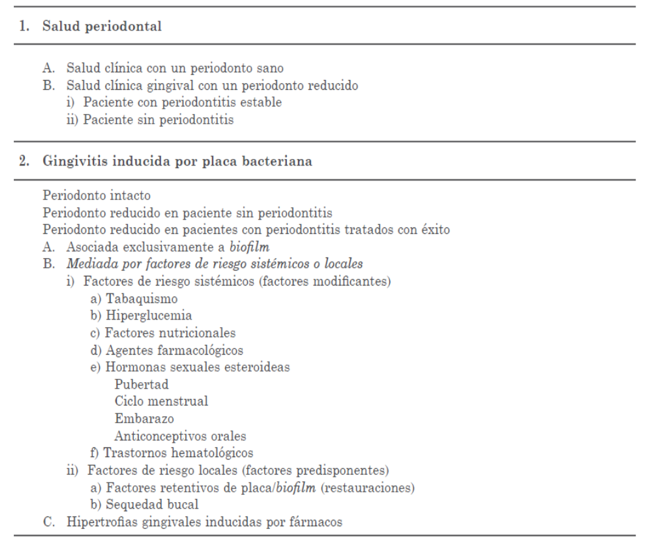
Figura 1. Clasificación de salud y gingivitis inducida por placa bacteriana
En cuanto a la parte de periodontitis: “…se tomó la decisión de cambiar el enfoque, reuniendo las periodontitis agresiva y crónica en una misma categoría y, al mismo tiempo, caracterizarla adicionalmente con un sistema de calificación por estadios y grados. La estadificación dependerá de la gravedad de la enfermedad y la complejidad prevista de su tratamiento, y los grados informarán sobre el riesgo de progresión de la enfermedad y de obtención de malos resultados en el tratamiento, junto con los posibles efectos negativos sobre la salud sistémica…”. Como se describe en la figura 2 y 3.
Con respecto a los puntos 3) Trastornos del desarrollo y adquiridos y manifestaciones periodontales de enfermedades sistémicas y 4) Patologías y condiciones periodontales, no se describen en el presente trabajo por exceder al mismo.
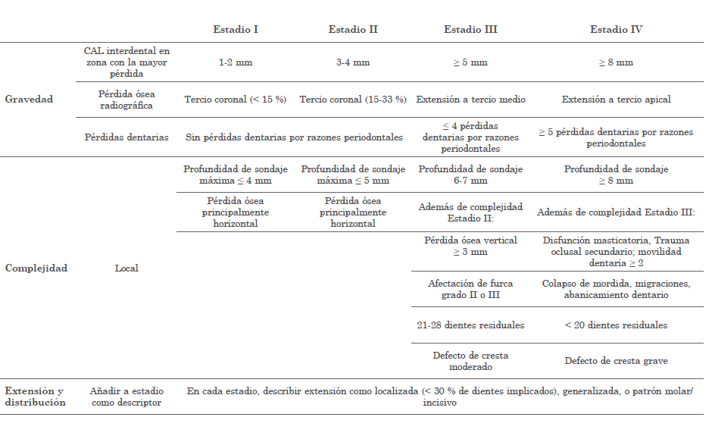
Figura 2. Clasificación de periodontitis por estadios
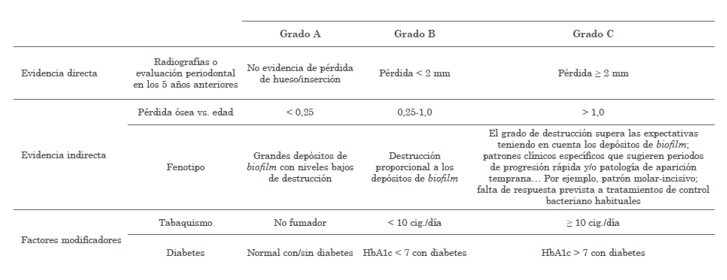
Figura 3. Clasificación de periodontitis por grados
CONCLUSIONES
El análisis realizado sobre la influencia de los anticonceptivos orales y las hormonas esteroideas en la salud bucal evidenció la relevancia de estas variables en la modulación de la gingivitis inducida por placa bacteriana y la progresión de la enfermedad periodontal. La cavidad bucal, como un nicho microbiano dinámico, responde a los cambios hormonales que pueden favorecer alteraciones inflamatorias e infecciosas, destacando la necesidad de abordar estos factores en la práctica odontológica.
Los hallazgos confirman que las hormonas sexuales, como los estrógenos y la progesterona, desempeñan un papel crucial en la respuesta inflamatoria del huésped. Estas hormonas no solo exacerban la inflamación gingival durante ciclos hormonales específicos, como el embarazo o la pubertad, sino que también modulan la composición del microbioma periodontal, favoreciendo el crecimiento de microorganismos patógenos. En el caso de los anticonceptivos orales, su uso se asoció con una mayor susceptibilidad a la inflamación gingival y la progresión de la periodontitis en determinados contextos clínicos.
La nueva clasificación de enfermedades periodontales de la AAP y la EFP aporta herramientas valiosas para caracterizar con mayor precisión estas patologías, diferenciando estadios y grados que facilitan la evaluación del impacto hormonal en la salud periodontal. Esta clasificación también resalta la interacción entre factores locales y sistémicos en la progresión de la enfermedad periodontal, consolidando la importancia de un enfoque interdisciplinario para su manejo.
En conclusión, el impacto de las hormonas esteroideas y los anticonceptivos orales en la salud periodontal subraya la necesidad de incorporar evaluaciones personalizadas en los planes de tratamiento. Los resultados obtenidos destacan la importancia de un monitoreo riguroso en pacientes con factores hormonales predisponentes y el diseño de estrategias preventivas adaptadas a cada etapa hormonal. Estos hallazgos abren la puerta a futuras investigaciones orientadas a optimizar el diagnóstico, manejo y prevención de las enfermedades periodontales en relación con factores hormonales.
REFERENCIAS BIBLIOGRÁFICAS
1. Ademe M, Girma F. Candida auris: From multidrug resistance to pan-resistant strains. Infect Drug Resist. 2020;13:1287–94.
2. Avila M, Ojcius DM, Yilmaz O. The oral microbiota: living with a permanent guest. DNA Cell Biol. 2009;28(8):405–11.
3. Benito B, Aranda S, López F, de la Rosa E, Rosas R, Sánchez L. Oral Candida isolates and fluconazole susceptibility patterns in older Mexican women. Arch Gerontol Geriatr. 2016;65:204–10.
4. Borgo P, Rodrigues V, Feitosa A, Xavier K, Avila-Campos M. Association between periodontal condition and subgingival microbiota in women during pregnancy: a longitudinal study. J Appl Oral Sci. 2014;22(6):528–33.
5. Brusca M, Verdugo F, Amighini C, Albaina O, Moragues M. Anabolic steroids affect human periodontal health and microbiota. Clin Oral Investig. 2014;18(6):1579–86.
6. Brusca M, Rosa A, Olatz A, Moragues M, Verdugo F, Pontón J. The impact of oral contraceptives on women’s periodontal health and the subgingival occurrence of aggressive periodontopathogens and Candida species. J Periodontol. 2010;81(7):1010–8.
7. Bulacio L, Paz M, Ramadan S, et al. Oral infections caused by yeasts in patients with head and neck cancer undergoing radiotherapy: Identification of the yeasts and evaluation of their antifungal susceptibility. J Mycol Med. 2012;22(4):348–53.
8. Carrillo de Albornoz A, Figuero E, Herrera D, Bascones A. Gingival changes during pregnancy: I. Influence of hormonal variations on clinical and immunological parameters. J Clin Periodontol. 2010;37(3):220–9.
9. Corgel J. Dental management of the female patient. J Clin Periodontol 2000. 2013;61:219–31.
10. Cuya-García R, Chávez-Raymi A, Flores-Culqui S, Párraga-Navarro M, Quinto-Benalcázar R, Tafur-Vásquez O. Enfermedad periodontal asociada al embarazo. Rev Cient Odontol (Lima). 2019;7(1):132–9.
11. De La Torre J, Quindos G, Marcos-Arias C, Marichalar-Mendia X, Gainza ML, Eraso E, et al. Oral Candida colonization in patients with chronic periodontitis: Is there any relationship? Rev Iberoam Micol. 2018;35:134–9.
12. GBD 2016 Disease and Injury Incidence and Prevalence Collaborators. Global, regional, and national incidence, prevalence, and years lived with disability for 328 diseases and injuries for 195 countries, 1990–2016: A systematic analysis for the Global Burden of Disease Study 2016. Lancet. 2017;390(10100):1211–59.
13. Jain M, Shah R, Chandolia B, et al. The oral carriage of Candida in oral cancer patients of Indian origin undergoing radiotherapy and/or chemotherapy. J Clin Diagn Res. 2016;10(2):17–20.
14. Javed F, Al-Kheraif A, Kellesarian S, Vohra F, Romanos G. Oral Candida carriage and species prevalence in denture stomatitis patients with and without diabetes. J Biol Regul Homeost Agents. 2017;31(2):343–6.
15. Jenkinson HF, Lamont RJ. Oral microbial communities in sickness and in health. Trends Microbiol. 2005;13(12):589–95.
16. Jewtuchowicz VM, Mujica MT, Malzone MC, Cuesta A, Brusca MI, Nastri ML, et al. Origin of the colonization of Candida dubliniensis in subgingival biofilm in immunocompetent subjects by RAPD-PCR assay. J Oral Microbiol. 2009;1(1):507.
17. Jewtuchowicz VM, Mujica MT, Brusca MI, Sordelli N, Malzone MC, Pola SJ, et al. Phenotypic and genotypic identification of Candida dubliniensis from subgingival sites in immunocompetent subjects in Argentina. Oral Microbiol Immunol. 2008;23(6):505–9.
18. Jewtuchowicz VM, Brusca MI, Mujica MT, Gliosca LA, Finquelievich JL, Iovannitti CA, Rosa AC. Subgingival distribution of yeast and their antifungal susceptibility in immunocompetent subjects with and without dental devices. Acta Odontol Latinoam. 2007;20:17–22.
19. Melton J, Redding S, Kirkpatrick W, et al. Recovery of Candida dubliniensis and other Candida species from the oral cavity of subjects with periodontitis who had poorly controlled type 2 diabetes: A pilot study. Spec Care Dentist. 2010;30(6):230–4.
20. Muthular M, Bálsamo F, Passero P, Jewtuchowicz V, Miozza V, Villalba MB, et al. Effects of tamoxifen on periodontal disease and Candida albicans of patients with breast cancer and other pathologies. Future Microbiol. 2019;14:129–37.
21. Newman MG, Takei HH, Klokkevold PR, Carranza FA. Newman and Carranza’s Clinical Periodontology. 13th ed. Philadelphia: Elsevier Health Sciences; 2019.
22. Mitova N, Rashkova M. Sex hormones in the saliva and periodontal health of children in puberty. J IMAB. 2019;25(4):2874–8.
23. Pazmiño VFC, Assem NZ, Pellizzer EP, De Almeida JM, Theodoro LH. Influencia del estrógeno en la enfermedad periodontal: Revisión de literatura. Av Periodon Implantol. 2015;27(2):75–8.
24. Preshaw P. Oral contraceptives and the periodontium. J Clin Periodontol 2000. 2013;61:125–59.
25. Rodríguez L, Rosa A, Rodríguez J, et al. The oral cavity: A reservoir that favors colonization and selection of Candida parapsilosis sensu stricto strains with high pathogen potential under conditions of gingival-periodontal disease. J Dent Sci Ther. 2017;2(1):1–6.
26. Rodríguez L, Jewtuchowicz V. Molecular characterization of Candida parapsilosis species complex in niches of the oral cavity in a cohort of patients from Argentina with different oral and dental clinical manifestations. J Dent Sci Ther. 2016;1(1):18–25.
27. Seneviratne CJ, Jin L, Samaranayake LP. Biofilm lifestyle of Candida: A mini review. Oral Dis. 2008;14(6):582–90.
28. Silk H. Diseases of the mouth. Prim Care. 2014;41(1):75–90.
29. Terças A, Marques S, Monteiro C, et al. Antifungal drug susceptibility of Candida species isolated from HIV-positive patients recruited at a public hospital in São Luis, Maranhão, Brazil. Front Microbiol. 2017;8:298.
30. Theill L, Dudiuk C, Morales-Lopez S, Berrio I, Rodríguez JY, Marin A, et al. Single-tube classical PCR for Candida auris and Candida haemulonii identification. Rev Iberoam Micol. 2018;35(2):110–2.
31. Truong T, Pang LM, Rajan S, Wong SSW, Fung YME, Samaranayake L, et al. The proteome of community living Candida albicans is differentially modulated by the morphologic and structural features of the bacterial cohabitants. Microorganisms. 2020;8(10):1541.
32. Yap M, Alnuaimi A, Adams G, McCullough M. Oral candidal carriage in asymptomatic patients. Aust Dent J. 2016;61(2):190–5.
33. Herrera D, Figuero E, Shapira L, Jin L, Sanz M. La nueva clasificación de enfermedades periodontales y periimplantarias. Rev Cient Soc Esp Periodoncia. 2018;11:1–8.
34. Looney WJ, Muhlemann K, Narita M. Stenotrophomonas maltophilia: An emerging opportunistic human pathogen. Lancet Infect Dis. 2009;9(5):312–23.
35. Jun L, Ying L, Yu Z, Changzheng W, Benyan W, Jun W. Actinomyces and alimentary tract diseases: A review of its biological functions and pathology. Biomed Res Int. 2018;2018:3820215.
36. Santarelli A, Mascitti M, Galeazzi R, Marziali A, Busco F, Procaccini M. Oral ulcer by Sphingomonas paucimobilis: First report. Int J Oral Maxillofac Surg. 2016;45(3):1–5.
37. Handschuh-Briones RA, Silva-Arcos EN, Urrutia M, Godoy-Martínez P. Actividad antifúngica de los enjuagues bucales frente a Candida albicans y Rhodotorula mucilaginosa: Un estudio in vitro. Rev Iberoam Micol. 2020;37(2):78–83.
FINANCIACIÓN
Ninguna.
CONFLICTO DE INTERESES
Los autores declaran que no existe conflicto de intereses.
CONTRIBUCIÓN DE AUTORÍA
Conceptualización: Edward Alejandro Hansen.
Curación de datos: Edward Alejandro Hansen.
Análisis formal: Edward Alejandro Hansen.
Investigación: Edward Alejandro Hansen.
Metodología: Edward Alejandro Hansen.
Administración del proyecto: Edward Alejandro Hansen.
Recursos: Edward Alejandro Hansen.
Software: Edward Alejandro Hansen.
Supervisión: Edward Alejandro Hansen.
Validación: Edward Alejandro Hansen.
Visualización: Edward Alejandro Hansen.
Redacción – borrador original: Edward Alejandro Hansen.
Redacción – revisión y edición: Edward Alejandro Hansen.