doi: 10.56294/hl2023260
ORIGINAL
Normolipid-lowering effect of omegas in chia seed (Salvia hispanica) in wistar rats
Efecto normolipemiante de los omegas presentes en la semilla de chía (Salvia hispánica) en ratas wistar
Francisca Patricia Jimenez Granizo1 ![]() *, Glenda Marcela
Sarmiento Tomalá1
*, Glenda Marcela
Sarmiento Tomalá1 ![]() *, Zoraida Burbano Gómez1
*, Zoraida Burbano Gómez1 ![]() *, Alondra Idrovo Encalada1
*, Alondra Idrovo Encalada1 ![]() *, Pilar Asunción Soledispa Cañarte1
*, Pilar Asunción Soledispa Cañarte1 ![]() *, Alexandra López Barrera1
*, Alexandra López Barrera1 ![]() *
*
1Universidad de Guayaquil, Facultad de Ciencias Químicas. Guayaquil, Ecuador.
Citar como: Jimenez Granizo FP, Glenda Marcela ST, Burbano Gómez Z, Idrovo Encalada A, Soledispa Cañarte PA, López Barrera A. Normolipid-lowering effect of omegas in chia seed (Salvia hispanica) in wistar rats. Health Leadership and Quality of Life. 2023; 2:260. https://doi.org/10.56294/hl2023260
Enviado: 03-05-2023 Revisado: 19-07-2023 Aceptado: 14-10-2023 Publicado: 15-10-2023
Editor:
PhD.
Prof. Neela Satheesh ![]()
Autor para la correspondencia: Francisca Patricia Jimenez Granizo *
ABSTRACT
Chia seed (Salvia hispánica) constitutes a great nutritional value for considerable content of fiber, protein and polyunsaturated fatty acids, essential to keep a lipid proper health. According to studies made, it has been shown that omegas 3, 6, and 9 contained in chia contribute to improve the lipidic profile by exerting a normolipemic effect on it. The study herein evaluated the normolipemic effect of the chia seed oil, for which 6 groups of 7 rats were formed, the control group (CN) maintained a pellet base diet, of these, 5 groups were previously induced to a hypercholesterolemia with a fat rich diet for two months: one group was treated with atorvastatin (CP), 3 groups were treated with chia at concentrations of 250, 500, and 1000 mg/kg (C250, C500, C1000, respectively); a group maintained the fat rich diet (CD) until the end of the treatment. Lipid profile analysis were performed at 7, 14 and 21 days from the start of the treatment. The results showed that after 7 days the C1000 reduced its LDL and increased its HDL, showing no significant difference with the atorvastatin. At the end of day 21 the lipid profile levels improved at all doses of chia, having lower levels of cholesterol, triglycerides, LDL and HDL levels being higher, even above the CN, showing significant difference with the CD, with a statistical probability of (p <0,05).
Keywords: Chia; Omegas; Atorvastatin; Cholesterol; Triglycerides; HDL; LDL; Normolipemic.
RESUMEN
La semilla de chía (Salvia hispánica) constituye un gran aporte nutricional por su gran contenido de fibras, proteínas y ácidos grasos poliinsaturados, indispensables para mantener una salud lipídica adecuada. De acuerdo a estudios realizados se ha demostrado que los omegas 3, 6 y 9 contenidas en la chía, contribuye a mejorar el perfil lipídico ejerciendo un efecto normolipemiante sobre él. El presente estudió evaluó el efecto normolipemiante del aceite de la semilla de chía, para lo cual se realizaron 6 grupos de 7 ratas cada uno, el grupo control normal (CN) mantuvo una dieta a base de pellets, de estos, 5 grupos fueron inducidos previamente a hipercolesterolemia con una dieta rica en grasas durante 2 meses: un grupo fue tratado con atorvastatina (CP), 3 grupos fueron tratados de chía a concentraciones de 250, 500 y 1000 mg/kg (C250, C500, C1000 respectivamente); un grupo se mantuvo con la dieta rica en grasas (CD) hasta el final del tratamiento. Se realizaron análisis del perfil lipídico a los 7, 14 y 21 días de iniciado el tratamiento. Los resultados demostraron que a los 7 días la C1000 redujo el LDL y aumentó el HDL, no presentando diferencia significativa con la atorvastatina. Al término del día 21 los niveles del perfil lipídico se vieron mejorados en todas las dosis de chía, teniendo concentraciones menores de colesterol, triglicéridos, LDL y siendo mayores los niveles de HDL, incluso por encima del CN, mostrando diferencia significativa con el CD, con una probabilidad estadística (p < 0,05).
Palabras clave: Chía; Omegas; Atorvastatina; Colesterol; Triglicéridos; HDL; LDL; Normolipemiante.
INTRODUCCIÓN
Procesos de globalización y de desarrollo, así como un estilo de vida urbano
Industrializado, sedentarismo, la llamada transición nutricional (dietas pocos saludables) en los que se ha cambiado la dieta rica en vitaminas y minerales preparados con métodos tradicionales, por aquellos alimentos que han sido procesados y producidos industrialmente, ricos en grasas y calorías; conforman factores de riesgos que conllevan al síndrome metabólico relacionado con la prevalencia de enfermedades crónicas cardiometabólicas no transmisibles: diabetes mellitus, resistencia a la insulina, dislipemia, hipertensión arterial.(1,2,3,4,5,6,7,8,9)
Estas enfermedades constituyen los padecimientos crónicos no transmisibles que registran la mayor cantidad de enfermos alrededor del mundo.
La alta incidencia de las enfermedades crónicas cardiometabólicas no transmisibles, posee especial importancia por su asociación directa con enfermedad, discapacidad, muerte y por los altos costos que el sistema sanitario debe considerar para su control.(10,11,12,13,14,15,16,17,18)
En los últimos 20 años la prevalencia de la obesidad, sobrepeso se ha incrementado tanto en países desarrollados como en vía de desarrollo, esta epidemia está directamente relacionada en un alto porcentaje con personas que padecen de diabetes. Según la Organización Mundial de la Salud estimó que de seguir la tendencia de incremento, hasta el 2020 habrá aproximadamente 2 mil 300 millones de adultos con sobrepeso y más de 700 millones con obesidad.(19,20,21,22,23,24,25,26,27)
En América Latina la obesidad y sobrepeso se está incrementando de manera vertiginosa más que América del Norte o en Europa. La prevalencia de adultos obesos en 2008 se encuentra en México y Venezuela, con un porcentaje mayor al 30 %, Argentina, Chile, Guatemala, Ecuador del 20- 29 %, seguidos de Brasil, Colombia, Perú, Paraguay y Uruguay del 10 -19 %.(28,29,30,31,32,33,34,35,36)
La incorporación de la medicina alternativa tradicional al conocimiento médico en el futuro dependerá del grado de corroboración experimental para el desarrollo de fitofármacos, generando información sobre la evaluación de las propiedades curativas que poseen los omegas presentes en la chía que actúan regulando los valores del perfil lipídico en ratas dislipídicas, lo que conlleva a realizar la siguiente propuesta de investigación, la misma que está basada en la búsqueda de la comprobación de la eficacia que presenta esta variedad vegetal sobre la actividad terapéutica como normolipemiante.(37,38,39,40,41,42,43,44,45)
El presente estudio consta de las siguientes partes: al inicio tenemos lo referente a los objetivos que se realizaron, para la consecución final de la hipótesis sugerida, se encuentran las variables a medir para la determinación sobre la eficacia que posee la chía como tratamiento. En el primer capítulo encontramos el marco teórico y antecedentes, requeridos para la fundamentación científica de esta investigación. En tanto que, el capítulo 2 contiene la metodología, el tipo de investigación que se utilizó de carácter experimental, los métodos que se utilizaron para cuantificar ácidos grasos, omegas, comprobación de efecto normolipídico, etc. El análisis de resultados que consta en el capítulo 3 y que contiene a partir del análisis estadístico con la aplicación de ANOVA, la significancia estadística entre grupo que es lo que permitirá llegar a las conclusiones y que corresponde a la respuesta de cada objetivo específico planeado.(46,47,48,49,50,51,52,53)
¿La administración de los diferentes niveles de dosis del aceite de chía que contiene omegas 3, 6 y 9, permitirá establecer el tratamiento de mayor actividad terapéutica que actúa normalizando las concentraciones del perfil lipídico en los animales de experimentación?(54,55,56)
Objetivo General
Evaluar el efecto normolipemiante de los omegas presentes en la semilla de chía (Salvia hispánica) en ratas Wistar.
MÉTODO
Variables
Dependientes
Niveles de colesterol.
Niveles de triglicéridos.
Niveles de HDL-Colesterol.
Niveles de LDL-Colesterol.
Independientes
Dosis administrada de Salvia hispánica (mg/kg).
Tiempo de administración (días).
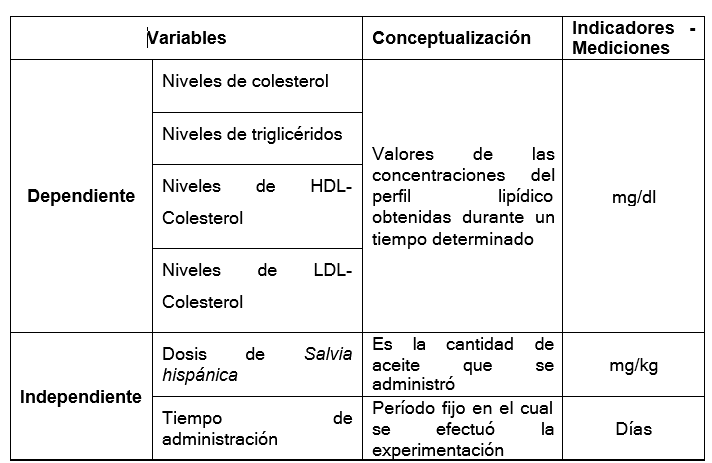
Figura 1. Operacionalización de las variables
El método teórico empleado es de carácter Hipotético – deductivo, cuantitativo, puesto que la investigación está basada en el planteamiento de una hipótesis, en donde existe variables a medir como el perfil lipídico y que de acuerdo a los resultados obtenidos podremos refutar o confirmar el efecto normolipemiante de la chía a través de los omegas presentes en dicha semilla.
Métodos empíricos
Se basa en el método observacional - experimental dado que se realizó desde análisis de control de calidad de la semilla de chía, la extracción del aceite de la semilla, la selección y conformación de grupos de animales de experimentación, así como también la inducción de dislipidemia a través de la preparación de una dieta rica en grasa y determinaciones serológicas del perfil lipídico durante días ya establecidos.
Métodos matemáticos o estadísticos
Se realiza análisis estadísticos de los datos obtenidos de las concentraciones de colesterol, triglicéridos, LDL, LDH; con el empleo de media y de desviación estándar, a partir del cual se realiza comparación de medias lo que nos permitirá establecer si existen diferencias significativas entre los diferentes grupos tratamientos.
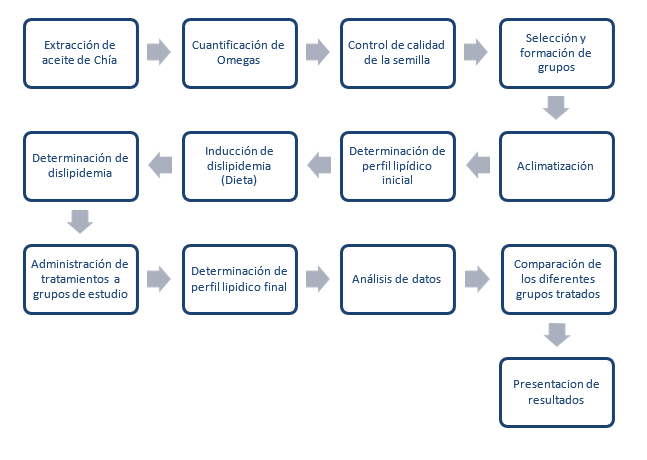
Figura 2. Secuencia de acción
La presente investigación está enmarcada en un estudio de tipo correlacional, dentro de este proceso existen variables tanto dependientes (niveles de colesterol, triglicéridos HDL y LDL) como independientes (dosis administradas 250-500-1000 mg/dl y el tiempo de administración), para evaluar los resultados se hace uso del análisis estadístico de los datos, para determinar dosis y tiempo en que el tratamiento presenta mejor efecto terapéutico.
Diseño experimental de la Investigación
Diseño experimental verdadero
Diseño de series cronológicas
El diseño del siguiente estudio es el diseño experimental verdadero, siguiendo un orden cronológico, motivo por el cual se trabajó con varios grupos de experimentación cuyo tiempo de tratamiento duró 21 días, realizando las mediciones cada 7 días.
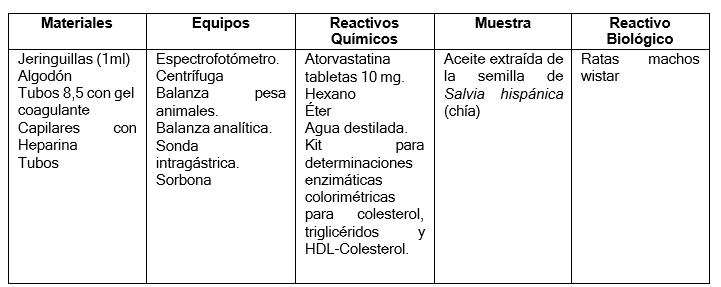
Figura 3. Datos de laboratorio
Adquisición de la especie
La obtención de semilla de chía se realizó mediante la compra en los supermercados de la ciudad de Guayaquil. Las semillas fueron llevadas al laboratorio de Fitoquímica y farmacognosia, además el laboratorio de Orgánica I, para realizar la extracción del aceite de chía mediante el método de soxhlet. Luego se procedió a la recuperación del solvente en el laboratorio de PROGECA, así como también el control de calidad; además en el laboratorio de Alimentos se efectuó el análisis de proteínas de la semilla; estos laboratorios pertenecen a la Universidad de Guayaquil – Facultad de Ciencias Químicas.
Extracción de aceite: Método de Soxhlet
Se pesó aproximadamente 50 gramos de semilla molida de chía, la cual fue colocada en un recipiente que consistía en un dedal elaborado con papel filtro y un tapón de algodón en la parte superior, junto al equipo de soxhlet se conectó un balón de base plana que contenía 500 ml de solvente (hexano), se calentó a 500C y se realizaron aproximadamente 15 sifonadas, las cuales en se realizaron durante 2 horas aproximadamente.
Perfil de ácidos grasos de la semilla de chía
Este análisis fue realizado en Laboratorios UBA, siguiendo el método de la AOCS Ce 1B-89.
Parámetros fisicoquímicos
Determinación del contenido de humedad
Se pesó 2 g ± 0,5 mg de semilla de chía y se transfirió a una cápsula de porcelana previamente tarada, se llevó a la estufa a 105 °C durante 3 horas. Pasado este tiempo se llevó las cápsulas hacia la desecadora donde se dejó enfriar a temperatura ambiente y se pesó. A continuación, se repitió el proceso anterior 1 hora más, hasta que se obtuvo una masa constante. Esta prueba se realizó por triplicado, (CIBE, 2015).
El resultado se obtiene mediante la siguiente fórmula:

Hg = Pérdida en peso por desecación (%).
M2 = Masa de la cápsula con la muestra de ensayo (g).
M1 = Masa de la cápsula con la muestra de ensayo desecada (g) M = Masa de la cápsula vacía (g).
100 Factor matemático.
Cenizas totales
Se pesó alrededor de 2-3 gramos de semilla en un crisol de porcelana tarado previamente. Las muestras (3) se llevaron a calentar hasta carbonizar en una mufla a una temperatura de 700 - 750 °C durante 3 horas, en el desecador se llevó a temperatura ambiente. Se repitió el proceso hasta que las muestras alcanzaron masa constante, (CIBE, 2015).
Los resultados se expresan de la siguiente manera:
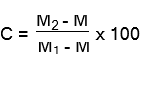
C = Porcentaje de cenizas totales en base hidratada M = Masa del crisol vacío (g)
M1 = Masa del crisol con la porción de ensayo (g) M2 = Masa del crisol con la ceniza (g)
100 = Factor matemático para los cálculos.
Densidad
Se pesó el picnómetro vacío y seco se registra su peso, luego se coloca agua dentro del picnómetro ajustando el nivel del líquido hasta ocupar toda el área del picnómetro extrayendo el exceso y secando exteriormente el picnómetro. Se pesó el picnómetro y se repitió la operación con la porción de muestra (aceite de chía) (CIBE, 2015).
Expresión de resultados
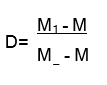
Dónde
M1 = Peso del picnómetro con la muestra (g) M2 = Peso del picnómetro con el agua (g).
M = Peso del picnómetro vacío.
Determinación de grasas
Se pesó 2 gramos de muestra de semilla molida de chía en fiolas, se agregó 20 ml de solvente (éter etílico) y se sometió al calor por aproximadamente 5 minutos, transcurrido este tiempo se dejó enfriar y se transfirió el líquido sobrenadante a cápsulas previamente taradas. Se evaporó el solvente contenido en las cápsulas a través de la estufa y luego llevado al desecador para posteriormente pesarlas hasta alcanzar peso constante (CIBE, 2015).
El porcentaje de grasas se determinó mediante la siguiente fórmula:
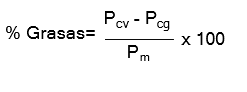
Dónde
Pcv = Peso de cápsula vacía
Pcg = Peso de cápsula más grasa Pm =Peso de la muestra
100 = Factor matemático para los cálculos
Determinación de fibra
Se pesó aproximadamente 2,5 g de la muestra de chía desengrasada, adicionó SO4H2 al 1,5 % (150 ml) se llevó a ebullición por 30 minutos, luego se enfrió, centrifugó, posteriormente se lavó de 4 a 5 veces con agua destilada, se transfirió el precipitado y se agregó 150 ml NaOH al 1,25 %, a continuación se procedió a hervir esta mezcla durante 30 minutos, se filtró con papel filtro y lavó 4 veces con agua.
En una cápsula de porcelana se recolectó el residuo y se determinó la muestra seca llevándola a la estufa a 105°C por 1 hora, se determinó a reducir a cenizas este residuo, en la mufla a 550°C por 30-40 minutos. Los valores obtenidos de muestra seca y cenizas, se resta y el valor resultante es la cantidad de fibra contenida en la muestra.
Los resultados se expresaron en porcentaje:
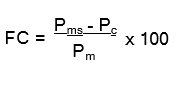
Donde
FC = Fibra cruda (%)
Pms = Peso de muestra seca (cápsula + fibra antes de ser llevada a la mufla) Pc = Peso de cenizas
Pm = Peso de muestra de semilla de chía (g)
Determinación de proteínas: Método Kjeldahl Digestión
Pesamos por diferencia en papel filtro o graso, una cantidad de muestra entre de 1 gramo aproximadamente de semilla de chía, se envolvió y se transfirió a un balón. Por otra parte se pesó 1 gramo de SO4Cu.5H2O y 18 gramos de SO4Na2 y se los añadió al balón. Al mismo tiempo se midió 25 ml de SO4H2 concentrado y se los agregó al balón, el mismo que fue colocado de forma inclinada en el reverbero del digestor, se calentó hasta que la muestra se carbonizo. Se mantuvo la muestra hirviendo hasta que se obtuvo un líquido claro y transparente y se mantuvo hirviendo durante 30 minutos más y se dejó enfriar. Se agregó 150 ml de agua destilada fría y hervida.
Destilación
En el destilador se colocó al final del tubo de desprendimiento un Erlenmeyer con 50 ml de solución de SO4H2 0,1 N y 2 gotas de solución indicadora de anaranjado de metilo, de tal manera que el extremo final del tubo de desprendimiento quedó introducido en la solución valorada de ácido, tomando en cuenta también que el agua estuvo circulando por el refrigerante.
Al balón completamente frío se agregó dos trozos de parafina para moderar la ebullición y evitar la espuma, luego se añadió lentamente 80 ml de soda Kjeldahl, procurando formar 2 capas de líquido, inmediatamente se agregó granallas de Zn y se insertó a la boca del balón el tapón de caucho que atravesó el extremo final de la trampa de seguridad del destilador.
Se abrió la llave de agua del refrigerante, se conectó el reverbero y se dejó que destile el amoniaco por 20 minutos aproximadamente. Para comprobar que se había desprendido todo el amoníaco se tomó la reacción del destilado en papel indicador rojo tornasol y si este no cambia a color azul, se comprueba que todo el amoníaco se desprendió.
Valoración
El destilado obtenido se tituló con NaOH 0,1 N valorado, para determinar los ml de SO4H2 que no se combinaron.
El resultado se obtiene mediante la siguiente fórmula:
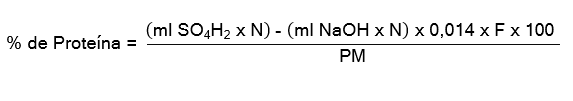
Donde
N = Normalidad de la solución.
0,014 = miliequivalente del Nitrógeno F = Factor de conversión de proteína PM = Gramos de muestra.
F= Factor de conversión del N (5,30).
Actividad normolipemiante
El método que siguió para realizar la evaluación de la actividad normolipemiante de la Chía fue el que se encuentra referenciado en el estudio realizado por el Departamento de Bioquímica de la Universidad del Litoral.
Bioensayo
Aclimatización de los animales de experimentación: Este estudio se realizó en las instalaciones del Bioterio de la Facultad de Ciencias Químicas de la Universidad de Guayaquil. En el área donde se mantuvo a los animales tuvieron condiciones ambientales idóneas que son requisitos indispensables para su normal desenvolvimiento. Dentro del bioterio existen condiciones establecidas para cada área, las mismas que se encuentran controladas y sus datos se encuentran registrados en los archivos del laboratorio. El requerimiento en cuanto a la temperatura fue de 22 0C±3, humedad 30 -70 %, y tuvieron un fotoperíodo de 12:12 (luz- oscuridad) mediante un sistema automatizado.
Los animales estuvieron colocados en jaulas plásticas con tapa, que sujeta el recipiente en el que se les colocó el agua, así como también el balanceado, para un mejor control cada animal fue codificado y, a cada jaula con su tratamiento se les colocó una tarjeta como identificación en el que constó la fecha de inicio y término de estudio, número de animales, tratamiento, prueba que se realizó.
Los animales que se utilizaron estuvieron comprendidos entre de 8 -12 semanas de edad. Para realizar este estudio se conformó 6 grupos cada uno de ellos tuvo 7 animales. Se procedió a pesar y se seleccionó aquellos animales que tenían un peso aproximado de 190 ± 20 g entre grupos.
Determinación colesterol y triglicéridos inicial. 18 horas antes de realizar la determinación se dejó en ayunas a los animales. Para realizar la extracción de sangre se anestesió al animal en una cabina saturada con éter etílico, se extrajo la sangre a nivel retroorbital utilizando un capilar y un tubo de ensayo en el cual se recogió la muestra, luego se regresó al animal a su jaula.
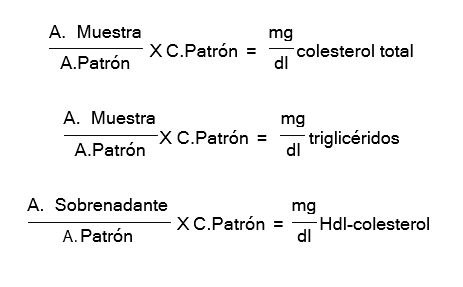
Se siguió la técnica de Linear Chemicals S.L para la determinación de colesterol, triglicéridos y Hdl-colesterol. Mientras que para Ldl-colesterol lo obtuvimos por diferencias.
Inducción de hipercolesterolemia: se les suministró una dieta hipercalórica rica en grasa. La inducción se la realizó de la siguiente manera en los diferentes grupos: al grupo Control Normal (1) se le suministró durante 60 días el balanceado normal. Mientras que a los grupos (2, 3, 4, 5, 6): se le suministró por 60 días la dieta rica en grasa saturada que consistió en la administración de los siguientes constituyentes de acuerdo a la tabla 2.
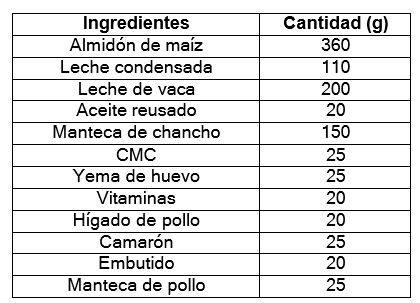
Figura 4. Constituyentes para la dieta hipercalórica
Para controlar el consumo diario la ración fue pesada, así como también el residuo. Comprobada el incremento de los valores de los componentes del perfil lipídico se procedió al suministro de los diferentes tratamientos. Se consideró que los niveles de colesterol y triglicéridos se encuentran incrementados cuando los valores estén entre (100 -150 mg/dl).
Administración de tratamientos: Para ello se procedió a la administración diaria por vía oral durante 21 días de todos los tratamientos de acuerdo a la dosis, que se encuentra detallada en la figura 5.
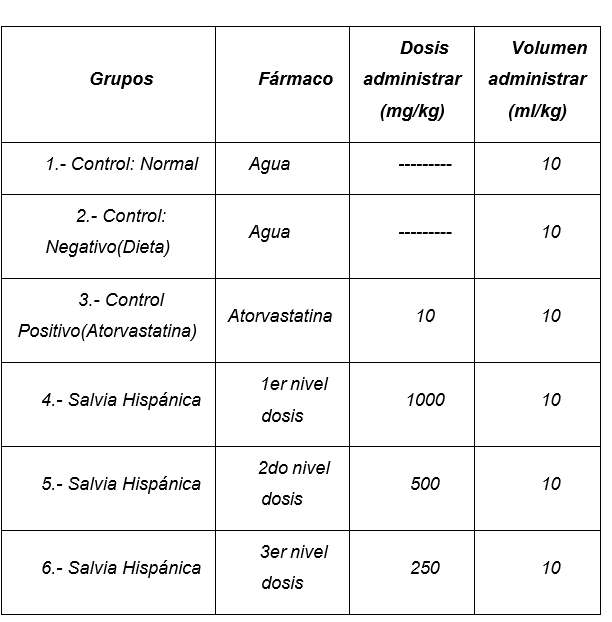
Figura 5. Tabla de Dosificación
A los grupos 1 (control normal) y 2 (control negativo) se procedió a la administración diaria de agua en un volumen de 10 ml /kg el mismo que fue recalculado para el peso del animal, diariamente por el lapso de 21 días. El grupo 2 recibió dieta hipercalórica por los días que duró la experimentación; en tanto que, el grupo control normal recibió el balanceado normal, el grupo 3 recibió el fármaco por 21 días de tratamiento en la dosis de 10 mg/kg por vía oral. Para la administración oral se sujetó el animal muy ligeramente sin ejercer mucha presión para no obstaculizar el paso de la sonda intragástrica, la misma que estaba acoplada a una jeringuilla que contenía el volumen para la administración de la dosis adecuada de acuerdo al peso corporal de la rata. A los siguientes grupos se le administró el aceite de chía en las dosis de 250- 500-1000 mg/kg en el volumen correspondiente durante los días que duró la experimentación (21 días). La vía de administración utilizada fue la oral.
Determinación de Colesterol, triglicéridos, HDL-colesterol y LDL- colesterol durante los días de prueba: Cada siete días de tratamiento hasta cumplir las tres semanas, se extrajo muestra de sangre para las determinaciones de colesterol, triglicéridos y Hdl-colesterol siguiendo las metodologías mencionadas anteriormente, tanto para la extracción como para la determinación.
Terminado el período de tratamiento (21 días), luego de haber realizado la última extracción se eliminó a los animales siguiendo los principios éticos con el fin de evitar el sufrimiento al animal.
RESULTADOS
Los resultados fueron elaborados en formato Excel, en el cual están las absorbancias y concentraciones de colesterol, triglicéridos y Hdl-colesterol iniciales, durante la dieta y finales.
Cálculos de los resultados
Se calculó el promedio de las concentraciones de colesterol, triglicéridos y Hdl- colesterol mediante la aplicación de la fórmula tanto para los valores iniciales y finales; además se calculó la desviación estándar de los mismos.
Análisis de los resultados
Se realizó un análisis de los datos de concentraciones mediante un programa estadístico, en el que se aplicó la comparación de medias.
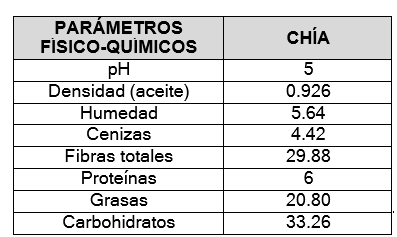
Figura 6. Parámetros físico-químicos
De acuerdo a la figura 6 muestra los porcentajes de cada uno de los parámetros medidos. En el caso de densidad y pH fue analizado en el aceite obtenido a partir de la extracción por soxhlet. Todos los análisis fueron realizados por triplicado.
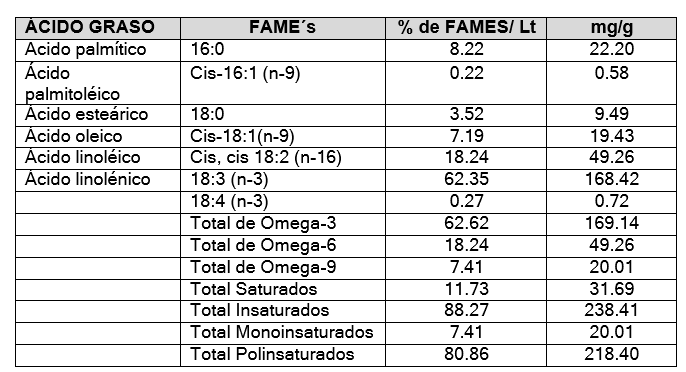
Figura 7. Perfil de ácidos grasos (Perfil de FAMES)
De acuerdo al análisis realizado del perfil de ácidos grasos de la semilla de chía se puede observar lo siguiente: el porcentaje del omega 3 es de 62,62 %, omega 6 presenta 18,24 % y el omega 9 comprende el 7,41 % con un total de ácido grasos insaturados de 88,27 %; además presenta otros aceites tales como el ácido palmítico con el 8,22 %, ácido palmitoléico con el 0,22 % y ácido esteárico con el 3,52 % dando un total de 11,73 % de ácidos grasos saturados.

Figura 8. Concentraciones iniciales de colesterol, triglicéridos, Hdl-colesterol y Ldl-colesterol
Al inicio del ensayo luego de una redistribución de los grupos se comprobó estadísticamente que los animales no presentaron diferencias significativas entre grupos, dando como promedio inicial de 35,11 ± 3,42 en cuanto a colesterol basal, anexo 15. los valores normales se encuentran por debajo de los parámetros establecidos de acuerdo a estudios realizados por Laboratorio Animal del profesor Thomas George, siendo las ratas Wistar los animales experimentales más empleados en trabajos científicos.
Así mismo los triglicéridos basales, las medias fueron comparadas estadísticamente, en la cual no presentaron diferencias significativas entre grupos, dando como promedio inicial de 36,93 ± 4,69; algunos estudios indican que no existe mayor diferencia entre el sistema cardiovascular entre las ratas y mamíferos incluyendo el hombre, lo que hace que sea un modelo viable para evaluar el perfil lipídico en dichos animales.
De la misma manera como el análisis estadístico anterior, luego de haber comparado las medias, se puede observar que todos los grupos tratados no presentan diferencias significativa, dando como valores un promedio inicial de 12,70 ± 0,91 para HDL- Colesterol. Las concentraciones de HDL se encuentran en valores mínimos, ya que ratas y mamíferos en estado de salubridad, tienden a mantener su medio interno constante bajo condiciones ambientales controladas.
En cuanto a LDL-Colesterol basal, se demostró en la fase inicial que no presentan diferencias significativas entre grupos, dando como promedio inicial de 15,18 ± 3,71. Las concentraciones de LDL basal se encuentran estrechamente relacionadas entre los grupos, puesto que se mantuvieron en período de adaptación bajo condiciones de humedad y luz controladas previo al análisis inicial figura 9.
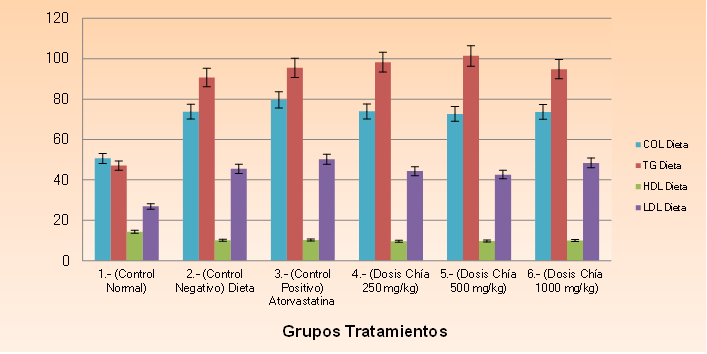
Figura 9. Concentraciones de colesterol, triglicéridos, Hdl-colesterol y Ldl- colesterol después de los 60 días de dieta
En esta fase, se estableció que los grupos que recibieron la dieta rica en grasas (60 días), los datos que corresponden a colesterol se incrementaron, estableciéndose diferencias significativas con el control normal que presentó un valor de (50,66 ± 3,82), para el control negativo # 2(73,78 ± 11,46), control positivo # 3 (79,63 ± 11,57), grupo # 4 (73,92 ± 14,56), grupo # 5 (72,68 ± 12,21), grupo # 6 (73,65 ± 11,34), cabe recalcar que todos los grupos fueron inducidos con la dieta a excepción del grupo control antes de iniciar el tratamiento con las diferentes dosis.
De acuerdo a la figura 9, en donde se puede observar que los valores de colesterol, están aumentados, debido al alto consumo de grasas saturadas, la cual se ha adquirido de manera exógena, es decir, por medio de la dieta hipercalórica administrada durante 2 meses por la que los lípidos de la dieta son transportados desde el intestino hasta el hígado y otros tejidos; estos lípidos al ser absorbidos, las células intestinales los empaca en quilomicrones (lipoproteínas de mayor tamaño), que también contienen triglicéridos, fosfolípidos, colesterol y apoproteinas incrementando de esta manera el colesterol en sangre.
Además, se puede observar, que las concentraciones de triglicéridos se elevaron en comparación a la concentración del grupo control normal dando como resultado (47,09 ± 8,08) mg/dl, mientras que en el grupo # 2 su valor es de (90,69± 15,72) mg/dl, en el grupo # 3 (95,5 ± 14,84) mg/dl, en el grupo # 4 (98,3 ± 15,64) mg/dl, en el grupo # 5 (101,44 ± 14,68) mg/dl y en el grupo # 6 (94,89 ± 15,55) mg/dl, mostrando de esta manera que existe diferencia significativa entre las medias. Esto se debe a que con la dieta se ingieren aproximadamente 100 g de lípidos que representa el 40 % del aporte calórico de esto, el 90 % son triglicéridos, acompañados por colesterol y esteroles vegetales.
Las concentraciones de HDL-colesterol disminuyeron en comparación a la concentración del grupo control normal dando como resultado (14,37 ± 1,88) mg/dl, mientras que en el grupo # 2 su valor es de (10,14 ± 0,67) mg/dl, en el grupo # 3 (10,28 ± 0,79) mg/dl, en el grupo # 4 (9,65 ± 0,84) mg/dl, en el grupo # 5 (9,75± 0,94) mg/dl y en el grupo # 6 (9,95 ± 0,71) mg/dl, mostrando de esta manera que existe diferencia significativa entre las medias (Anexo 16). La disminución de HDL en los grupos de dieta se debe porque los ésteres del colesterol de las HDL son reemplazados por triglicéridos reduciendo así la cantidad de colesterol transportado por las HDL en el camino reverso del colesterol, explicando de esta forma la relación entre la hipertrigliceridemia e hipoHDL.
Las concentraciones de LDL-colesterol aumentaron en todos los grupos excepto por el grupo control normal dando como resultado (26,87 ± 4,88) mg/dl, mientras que en el grupo # 2 su valor es de (45,51 ± 13,92) mg/dl, en el grupo # 3 (50,25 ± 12,28) mg/dl, en el grupo # 4 (44,36 ± 8,70) mg/dl, en el grupo # 5 (42,64 ± 12,33) mg/dl y en el grupo # 6 (48,43 ± 12,69) mg/dl, exponiendo de esta manera que existe diferencia significativa entre las medias, tal como se indica en el. Esto se debe a que el intercambio de ésteres del colesterol de las LDL por triglicéridos hace que estas LDL “ricas en triglicéridos” sean un buen sustrato para la HDL, la cual extrayendo triglicéridos de las LDL se transforma en partículas LDL llamadas “pequeñas y densas”, reconocidas por su poder aterogénico y por su ligazón fisiopatológica con la hipertrigliceridemia, en particular la que se presenta en los síndromes de resistencia a la insulina, como el síndrome metabólico o la diabetes tipo 2.
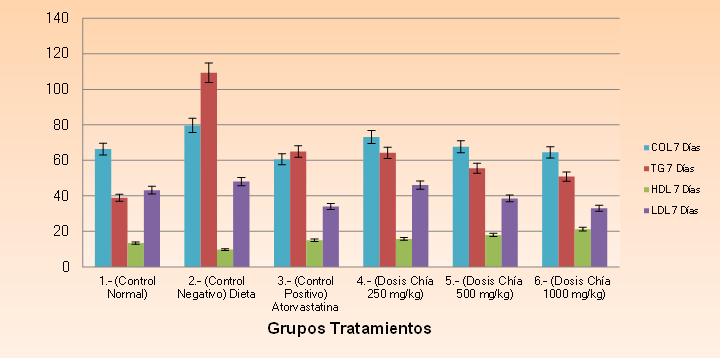
Figura 10. Concentraciones de colesterol, triglicéridos, Hdl-colesterol y Ldl- colesterol a los 7 días de tratamiento
A los 7 días de haber empezado el tratamiento con las diferentes dosis del aceite de chía, los grupos no presentaron diferencia significativa, mientras que el grupo del control negativo si presentó diferencia dando un valor de (79,68 ± 9,72) mg/dl frente a todos los grupos, debido a que este grupo se le sigue administrando la dieta rica en grasa saturada, motivo por el cual se encuentra aumentado el valor del mismo.
De acuerdo a lo observado figura 10 los niveles plasmáticos de colesterol en el control negativo son altos, a diferencia del grupo control normal y los grupos de tratamiento; una alta ingesta de colesterol en los alimentos conduce a una disminución de la producción endógena y viceversa, es decir el colesterol presente en el organismo solo es adquirido a través de la dieta (Gil-Hernández, 2010).
En cuanto a las concentraciones de triglicéridos se puede observar que a pesar de la disminución numérica no existe diferencia estadística en cuanto a los grupos de las diferentes dosis e incluso con el grupo control normal y el grupo control positivo, arrojando los siguientes valores para el grupo # 1 (48,57 ±9,68), grupo # 3 (65,04 ±18,3), grupo # 4 (64,27 ± 13,99), grupo # 5 (55,6 ± 9,79) y el grupo # 6 (50,88 ±19,23), sin embargo se puede observar que el grupo # 2 control negativo quien no recibió ningún tratamiento se mantuvo elevado con un valor de (109,37± 10,89) presentando diferencia significativa frente a todos los grupos.
Observando la figura 11, las concentraciones de LDL-colesterol disminuyeron en todos los grupos excepto por el grupo control negativo quien no tiene ningún tratamiento y está siendo sometido a la dieta rica en grasa saturada dando como resultado (48,06 ± 11,2) mg/dl de Ldl-Colesterol, demostrando que existe diferencia significativa entre las medias. Cabe mencionar que la atorvastatina reduce las concentraciones plasmáticas del colesterol y lipoproteínas en el hígado y la subsiguiente síntesis hepática del colesterol, aumentando el número de receptores para LDL en la superficie celular, incrementando su absorción y catabolismo.
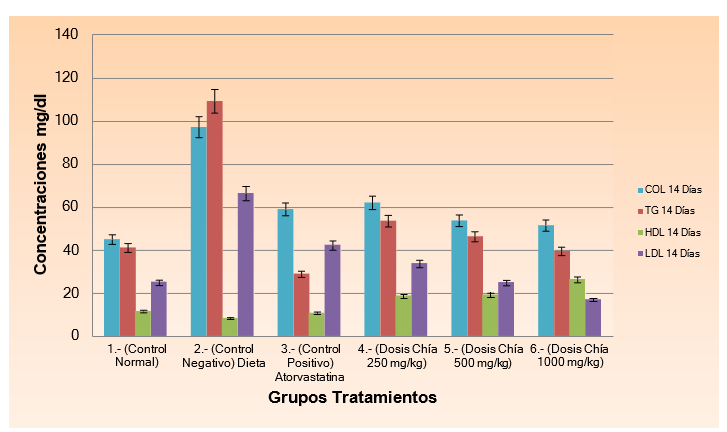
Figura 11. Concentraciones de colesterol, triglicéridos, Hdl-colesterol y Ldl- colesterol a los 14 días de tratamiento
A los 14 días de tratamiento según el anexo 18, reporta el grupo que no recibió tratamiento alguno (control negativo), una concentración de (97,03 ± 6,78) mg/dl de colesterol. Sin embargo el grupo tratado con la dosis de 1000 mg/kg guarda relación estadísticamente con el control normal, en tanto que el grupo tratado con 250 y 500mg /kg guardo proximidad con el control positivo (Atorvastatina). Tal como se puede observar en la figura 11.
En la determinación de HDL-colesterol se obtuvo que el grupo tratado con 1000 mg /kg de aceite aumentará el Hdl-colesterol (colesterol bueno) por lo tanto el nivel de significancia no se encuentra relacionado con ningún grupo entre sí, siendo su valor de (26,54 ± 3,04) mg/dl. Sin embargo el grupo tratado con la dosis de 250 mg/kg no tiene diferencia significativa con la dosis de 500 mg/kg.
Al observar la figura 11, la diferencia significativa de HDL entre las concentraciones del grupo control normal y control negativo frente a los grupos de tratamiento de chía, es debido a la ingesta del aceite del mismo que contienen acido alfa linolénico (ALA); su ingesta diaria previene síntomas de deficiencia; tanto la ingesta de ALA junto con otros ácidos grasos insaturados (Omega 6 y 9) es recomendado para ser parte de una dieta saludable (Organización de las Naciones Unidas para la Alimentación y la Agricultura, 2012).
Luego del análisis estadístico correspondiente, el grupo tratado con 500 mg /kg de aceite guarda relación con el grupo control normal, es decir, alcanzó un nivel similar, mientras que el grupo tratado con la dosis de 1000 mg/kg disminuyó el Ldl-colesterol (colesterol malo), siendo su valor de (17 ± 5,95) mg/dl. Anexo 18. Este efecto es debido a la presencia de ácido oleico, también existente en el aceite de chía, produciendo un efecto más marcado que el ácido linoleico; aumentando ligeramente el HDL y reduciendo la posible oxidación del LDL, todo esto produce mejorar el perfil lipídico y tiene un efecto positivo sobre la salud de los animales tratados.
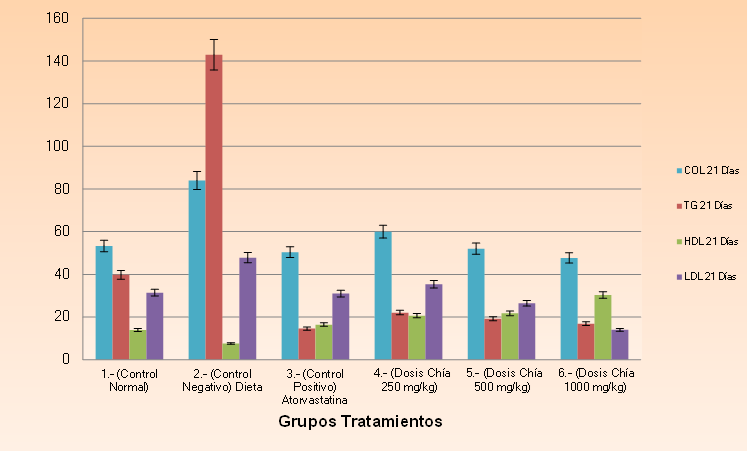
Figura 12. Concentraciones de colesterol, triglicéridos, Hdl-colesterol y Ldl- colesterol a los 21 días de tratamiento
El presente gráfico detalla las variaciones de los valores del perfil lipídico de los grupos administrados con los diferentes tratamientos a los 21 días.
A los 21 días de tratamiento se puede observar que las concentraciones de colesterol del grupo tratado con 1000 mg/kg de aceite disminuyó mucho más con respecto a todos los grupos, en cuanto al grupo control normal presentó una similitud con el grupo control positivo y con el grupo de dosis de 500 mg/kg, es decir, alcanzó un nivel similar. Anexo 19. La semilla de chía Tiene gran importancia debido a la presencia del ácido linolénico y linoléico, por su efecto hipocolesteromiante, que disminuye los niveles de colesterol total y LDL, influenciando positivamente sobre diversos factores de riesgo entre los que se encuentran las enfermedades cardiovasculares y las dislipemias.
En cuanto a las concentraciones de triglicéridos, el grupo tratado con 1000 mg/kg de aceite, el grupo tratado con 500 mg/kg y el control positivo presenta una similar significancia estadística. Cabe mencionar que el control negativo se mantiene elevada su concentración debido a que se le siguió administrando la dieta para que una vez finalizado el tratamiento se pueda realizar una comparación estadística en la cual se está comprobando la eficacia del aceite de chía. Anexo 19. Esta concentración elevada de triglicéridos es debido a que aproximadamente el 97 % de la grasa ingerida es absorbido, y un alto porcentaje de la misma penetra en la circulación a través del sistema linfático en forma de quilomicrones, los que a su vez se dirigen al tejido adiposo donde depositan los triglicéridos contenidos en la molécula.
Por otra parte se puede observar que en las tres dosis diferentes de chía hubo un aumento de HDL-Colesterol siendo de mayor nivel la dosis de 1000 mg/kg (30,31 ± 3,6) mg/dl. Además se puede observar que incluso es mayor que el grupo control normal y el grupo que fue tratado con Atorvastatina. Mientras por otra parte el grupo que solo se le administró la dieta se encuentra su nivel disminuido. Tal como se muestra en el anexo 19 y en la figura 12.
El aumento de HDL al día 21 de tratamiento, se debe al metabolismo del ácido oleico, linoléico y alfa linolénico, los cuales son elongados y desaturados por el sistema enzimático microsomal, que los transforma en derivados de mayor tamaño de cadena (hasta 24 carbonos en omegas 3 y 6) y con un mayor grado de instauración como en el caso del omega 3, produciendo así el efecto terapéutico esperado en las diferentes dosis de tratamiento.
La concentración de LDL-colesterol a dosis de 1000 mg/kg da un valor de (13,97 ±5,86) mg/dl, siendo la de mayor eficacia, observando además que existe diferencia significativa en comparación con los demás grupos, sin embargo, la dosis de 500 mg/kg también presenta disminución de Ldl-colesterol, la dosis de 250 mg/kg presenta una similitud estadística al grupo control normal y al grupo control positivo (Atorvastatina).
La recopilación de los datos a los 21 días de experimentación nos permite aceptar la hipótesis para ello se proporciona una respuesta acertada sobre la sugerida en el inicio de esta investigación.
CONCLUSIONES
De acuerdo a las determinaciones realizadas en el aceite de chía sobre el contenido total de ácidos grasos insaturados fue de 88 %; la presencia de estos ácidos (oleico, linoleico y linolénico) es la que le permite a la semilla de chía actuar sobre colesterol, triglicéridos, HDL, LDL, regulando los valores del perfil lipídico que se encuentran incrementados en los animales de experimentación por la administración diaria de una dieta hipocalórica, rica en ácidos grasos saturados.
Los resultados de los parámetros físico químicos realizados en la semilla de chía, fueron de un 5,64 % de humedad, 4,42 % de cenizas, 29,88 % de fibras totales, 6 % de proteínas, un 20,88 % de grasas y 33,26 % de carbohidratos. Los resultados de los parámetros básicos como humedad y cenizas concuerdan con el estudio. Por otra parte, el porcentaje de proteínas concuerda con lo declarado en la etiqueta del producto alimenticio. fibras totales y carbohidratos fue mayor que el análisis realizado por los autores ya mencionados.
Según los resultados obtenidos del perfil lipídico se puede deducir que las dosis trabajadas (250, 500,1000) mg/kg a los 7 días en cuanto a colesterol, triglicéridos no presentan disminución significativa, sin embargo en lo que respecta a HDL (colesterol bueno) a la dosis de 1000 mg/kg se incrementaron (21,29±4,09) estableciéndose diferencias estadísticas entre grupos.
En tanto que a los 14 días de tratamiento el comportamiento de las concentraciones de colesterol fue similar al día 7, excepto los valores de triglicéridos que a la dosis de 1000 mg/kg se encontraban disminuidos (39,47 ± 13,57) presentando semejanzas con el control normal (41,03 ±4,93). En cuanto a HDL a la dosis de 250, 500 y 1000 mg/kg se encontraban regulados y similares (18,88 ± 3,01; 19,36 ± 2,41; 26,54 ± 3,04) al control normal (11,6 ±1,46), mientras que el LDL (colesterol malo) sus valores se encontraban disminuidos en lo que respecta a los grupos tratados con CHIA (17 ±5,95) y Atorvastatina.
A los 21 días post tratamiento las dosis ensayadas (250, 500, 1000) mg/kg consiguieron regular los niveles de colesterol en todos los grupos (59,96 ± 4,99; 51,99 ± 3,22; 47,65 ± 3,76), en tanto que los triglicéridos (22,07 ± 49,43; 19,16 ± 7,53; 16,89 ± 6,96) y LDL (35,38 ± 5,51; 26,45 ± 2,45; 13,97 ± 5,86) revelaron valores que se encontraban incluso por debajo de los niveles que presentaban el grupo control normal (39,75 ± 5,89; 31,41 ± 6,86) respectivamente, el HDL se encontró incrementado los valores (20,59 ± 2,61; 21,71 ± 2,65; 30,31 ± 3,6) en relación al grupo control (13,95 ± 0,62). De lo que se puede concluir que a la dosis de 1000 mg/kg a los 7 días, la chía empezó a normalizar los valores de los animales dislipídicos, fueron regulando los valores paulatinamente y al termino del estudio (21 días) todas las dosis estudiadas (250, 500, 1000 mg/kg) consiguieron nivelar las concentraciones del perfil lipídico.
REFERENCIAS BIBLIOGRÁFICAS
1. Aje, T. O., y Miller, M. (2009). Cardiovascular disease: a global problem extending into the developing world. World journal of cardiology, 1(1), 3.
2. Antruejo A, Azcona JO, García PT, et al. (2011). Omega-3 enriched egg production: the effect of a-linolenic x-3 fatty acid sources on laying hen performance and yolk lipid content and fatty acid composition. British Poultry Science, 52(6):750–760. doi: 10.1080/00071668.2011.638621.
3. Ayerza, R. (1995). Oil content and fatty acid composition of chia (Salvia hispanica L.) from five northwestern locations in Argentina. Journal of the American Oil Chemists’ Society, 72, 1079-1081.
4. Ayerza, R., Wayne Coates. (2006). Chía, redescubriendo un olvidado alimento de los aztecas. Buenos Aires: Editorial del Nuevo Extremo
5. Ayerza, R, Coates, W. (2007) Effect of dietary α-linolenic fatty acid derived from chia when fed as ground seed, whole seed and oil on lipid content and fatty acid composition of rat plasma. Annals of Nutrition and Metabolism. 51(1), 27–34.
6. Barja, S., Barrios, X., Arnaiz, P., Domínguez, A., Villarroel, L., Castillo, O.,…Mardones, F. (2013).Niveles de lípidos sanguíneos en escolares chilenos de 10 a 14 años de edad. Nutr Hosp, 28(3), 719–725.
7. Bellido, C., López-Miranda, J., Blanco-Colio, LM., Pérez-Martínez, P., Muriana FJ., Martin-Ventura, JL., et al. (2004) Butter and walnuts, but not olive oil, elicit postprandial activation of nuclear transcription factor kappaB in peripheral blood mononuclear cells from healthy men. American Journal Clinical Nutrition, 80:1487- 91.
8. Burbano, Z. (2013). Prácticas de Laboratorio de Instrumental. Guayaquil.
9. Cuneo, C. (2001). Lipoproteínas de alta densidad (HDL) y enfermedad coronaria. Revista Federación Argentina de Cardiología, 30, 103-111. Recuperado de http://fac.org.ar/revista/01v30n1/cuneo/cuneo.PDF
10. Cahill, J. (2003). Ethnobotany of chia,Salvia hispanica L. (Lamiaceae).
11. Economic Botany, 57, 604-618.
12. Coronado M., V. y. (2006). Los Ácidos Grasos Omega-3 y Omega-6: Nutrición, Bioquímica y Salud. Obtenidode http://www.facmed.unam.mx/publicaciones/ampb/numeros/2006/03/e_AcidosGra sos.pdf
13. COLÉGIO BRASILEIRO DE EXPERIMENTAÇÃO ANIMAL (COBEA), Boletim informativo, vol.3, 2008, 10 p
14. Chicco, A., D´ Alessandro, M., Hein, G., Oliva, M., & Lombardo, Y. (2009). Dietary chia seed (Salvia hispanica L.) rich in a-linolenic acid improves adiposity and normalises hypertriacylglycerolaemia and insulin resistance in dyslipaemic rats. British Journal of Nutrition, 101(1), 41–50. doi: 10.1017/S000711450899053X
15. Censos, I. N. (2014). Tomo I Encuesta Nacional de Salud y Nutrición ENSANUT-ECU 2012. Obtenido de Ministerio de Salud Pública: http://www.ecuadorencifras.gob.ec/documentos/web- inec/Estadisticas_Sociales/ENSANUT/MSP_ENSANUT-ECU_06-10-2014.pdf
16. CIBE. (2015). Biotecnología para el desarrollo. Curso Teórico-Práctico
17. Discovery Dsalud, (2009). Las semillas de chía un alimento supercompleto. Ediciones MK3 S.L.
18. Da Silveira Castello Branco, A. C., Formiga Melo Diniz, M. F., Nóbrega De Almeida, R., Bandeira Santos, H., Mendes De Oliveira, K., Do Amaral Ramalho, J., Gómes Dantas, J. (2011). Parámetros Bioquímicos e Hematológicos de Ratos Wistar e Camundongos Swiss do Biotério Professor Thomas George. Revista Brasileira de Ciências da Saúde, 15(2), 209-214. doi: 10.4034/RBCS.2011.15.02.11
19. Desarrollo, S. N. (2013). Objetivos Nacionales para el Buen Vivir. Obtenido de http://www.buenvivir.gob.ec/objetivos-nacionales-para-el-buen-vivir
20. Da Silva, R., Aguiar, É., Alves, S., Teixeira, A., Nogueira, M., & Roberto, M. (2014). Características químicas y el potencial antioxidante de la chía chilena semillas y aceite (Salvia hispanica L.) . ELSEVIER, 1303-1305.
21. European Food Information Council. (2008). La importancia de los ácidos grasos omega-3 y omega-6. Obtenido de http://www.eufic.org/article/es/artid/La- importancia-de-los-acidos-grasos-omega-3-y-omega-6/
22. Elikir, G. (2012). Tratamiento del paciente con dislipemia. Curso de capacitación de posgrado a distancia síndrome metabólico y riesgo vascular (págs. 10 - 13). Argentina: FEPREVA.
23. Elikir, G. (s.f.). ENFOQUE TERAPÉUTICO ACTUAL DE LAS DISLIPIDEMIAS
24. Y PERSPECTIVAS FUTURAS. En R. Calandra, & M. Barontini, Fisiopatología molecular y clínica endocrinológica (págs. 1331-1347). Argentina: Eli Lilly Interamerica Sucursal Argentina.
25. Elikir, G., Cúneo, C., Lorenzatti, A., Schreier, L., Corral, P., Aimone, D., . . . Vilariño, J. (2014). Consenso de la Sociedad Argentina de lípidos sobre hipercolesterolemia familiar. Argentina.
26. Forgaguera J., Gómez G. (2004). Bioquímica. Universidad Estatal a Distancia, San José, Costa Rica. Págs. 120 a 128
27. García-Ríos A., M. M. (2009). Omega-3 y Enfermedad Cardiovascular: más allá de los factores de riesgo. Recuperado de http://www.nutricion.org/publicaciones/revistas/Revisi%C3%B3n_Omega-3_2009_1.pdf
28. Gil Hernández, A. (2010). Metabolismo lipídico tisular. Tratado de Nutrición: Bases Fisiológicas y Bioquímicas de la Nutrición (pp. 279-292). Madrid: Editorial Medica Panamericana.
29. Gatica, A. (2011). Ácidos Grasos EPA y DHA y su vital importancia en la nutrición humana. Indualimentos, 58-60.
30. Guevara-Cruz M, Tovar A., Aguilar-Salinas, C., et al. (2012). A Dietary Pattern Including Nopal, Chia Seed, Soy Protein, and Oat Reduces Serum Triglycerides and Glucose Intolerance in Patients with Metabolic Syndrome. The Journal of Nutrition. 42(1), 64-69.
31. Hernández-Gómez, J. A.; Miranda-Colin, S. & Pena-Lomeli, A. (2008). Cruzamiento natural de chia (Salvia hispanica L.). Rev. Chapingo Ser.Hortic [online], 14(3). Recuperado de http://www.scielo.org.mx/scielo.php?pid=S1027-152X2008000300015&script=sci_arttext
32. Hernández-Gómez, J.A. & Miranda-Colin, S., (2008). Caracterización morfología de la chía. Revista Fitotecnia Mexicana, 31 (2). ISSN: 0187-7380.
33. Hernando, M. & Sánchez, M. T. (2008). ATORVASTATINA en la prevención secundaria del ictus isquémico de origen aterotrombótico o lacunar. (Informe para la Comisión de Farmacia y Terapéutica del Hospital Clínico Universitario de Valladolid). Recuperado de http://gruposdetrabajo.sefh.es/genesis/informesgenesis/ATORVASTATINA_ICTU S_HCUV_1208.pdf
34. Hatami, M., Tohidi, M., Mohebi, R., Khalili, D., Azizi, F., y Hadaegh, F. (2012). Adolescent lipoprotein classifications according to National Health and Nutrition Examination Survey (NHANES) vs. National Cholesterol Education Program (NCEP) for predicting abnormal lipid levels in adulthood in a Middle East population. Lipids in health and disease, 11(1), 1–7.
35. Illian, T., Jason C. & Bishop, Phillip A. (2011). Omega-3 Chia Seed loading as a means of carbohydrate loading. Journal of Strength and Conditioning Research, 25(1), 61-65.
36. INEC. (2011). Anuario de estadísticas vitales: Nacimientos y defunciones. Recuperado de http://www.inec.gob.ec/estadísticas_sociales/nac_def_2011/anuario.pdf
37. Jin F, Nieman DC, Sha W, et al. (2010) Supplementation of milled chia seeds increases plasma ALA and EPA in postmenopausal women. Plant Foods For Human Nutrition, 67:105–110. doi: 10.1007/s11130-012-0286-0.
38. Jiménez, P., Masson, L., & Quiral, v. (2013). Composición química de semillas de chía, linaza y rosa mosqueta y su aporte en ácidos grasos omega-3. Scielo, 40(2), 155-160.
39. Jaramillo-Garcés, Y. (2013). La chía (Salvia hispánica L.), una fuente de nutrientes para el desarrollo de alimentos saludables. (Tesis inédita de maestría, Corporación Universitaria Lasallista). Recuperado de http://repository.lasallista.edu.co/dspace/bitstream/10567/1043/1/La_chia_salvia_ hispanica_L_desarrollo_alimentos_saludables.pdf
40. Leal, D. P. (2001). Bioquímica Estructural y Aplicada a la Medicina. Instituto Politécnico Nacional.
41. Lasunción, M. A., Gómez-Coronado, D. (2008). Metabolismo de los triglicéridos plasmáticos y su relación con la arteriosclerosis. Sociedad Española de Medicina Interna. [Versión de Elsevier Doyma]. Recuperado de https://www.fesemi.org/sites/default/files/documentos/publicaciones/capitulo- 1_3.pdf
42. Martha GC, N. D. (2012). A Dietary Pattern Including Nopal, Chia Seed, Soy Protein, and Oat Reduces Serum Triglycerides and Glucose Intolerance in Patients with Metabolic Syndrome. The Journal of Nutrition .
43. Mataix-Verdú, J. (2009). Lípidos. Nutrición y Alimentación Humana (pp. 61-91). Barcelona: Ergon. Recuperado de http://www.uco.es/master_nutricion/nb/Mataix%20educadores/lipidos.pdf
44. M.E. Oliva, M. F. (18 de Septiembre de 2013). Pubmed. Obtenido de http://www.ncbi.nlm.nih.gov/pubmed/24120122.doi:10.1016/j.plefa.2013.09.010
45. Mesa, E., Gómez, R., & Ampudia, J. (2013). Pioglitazona en el control glucémico, perfil lipídico y riesgo cardiovascular: revisión actualizada sobre sus beneficios y datos emergentes sobre su seguridad. ELSEVIER, 1-12.
46. Mishra A., Chaudhary A., Sethi S. (2004). Oxidized omega-3 fatty acids inhibit NF-kappaB activation via a PPAR alpha-dependent pathway. Arterioscler Thromb Vasc Biol, 24 (9), 1621-7. Recuperado de http://www.ncbi.nlm.nih.gov/pubmed/15231516
47. Muñoz, J. L. (2008). Mecanismos, función y obtención de alimentos enriquecidos con ácidos grasos Omega-3. Obtenido de Boletín Oncológico del área sanitaria de Teruel: http://www.boloncol.com/boletin-25/mecanismos- funcion-y-obtencion-de-alimentos-enriquecidos-con-acidos-grasos-omega-3.html
48. Nieman DC, Cayea EJ, Austin MD, Henson DA, McAnulty SR, Jin F. (2009). Chia seed does not promote weight loss or alter disease risk factors in overweight adults. Nutrition Research, 29(6):414–418. doi: 10.1016/j.nutres.2009.05.011.
49. Norlaily Mohd A, Swee Keong Y., Wan Yong H. et al. (2012). Promising Future of Chia, Salvia hispánica.doi: 10.1155/2012/171956.
50. Nutri-Facts. (21 de Mayo de 2012). Ácidos Grasos esenciales. Recuperado de http://www.nutrifacts.org/fileadmin/redacteur/pdf/PDF_At_a_Glance/ES/acidos_gr asos_esenciales.pdf
51. OMS. (2004). Portal de Información. Recuperado el 18 de Junio de 2015, de ONG Human Info: http://apps.who.int/medicinedocs/es/d/Js5422s/20.html
52. Organización de las Naciones Unidas para la Alimentación y la Agricultura. (2012). Grasas y ácidos grasos en nutrición humana. Recuperado de http://www.fao.org/docrep/017/i1953s/i1953s.pdf
53. Poveda, E., Ayala, P., Rodríguez, M., Ordoñez E., Baracaldo, C., Delgado, W., Guerra, M. (2005). Efecto del suplemento de aceites vegetales sobre el perfil lipídico en ratas Wistar. Revista Scielo, 25, 101-9. Recuperado de http://www.biblionline.ufpb.br/ojs/index.php/rbcs/article/viewFile/10800/6056
54. Pineda, C.A. (2008). Síndrome metabólico: definición, historia, criterios. Colombia Medica, 39 (1). Recuperado de http://colombiamedica.univalle.edu.co/index.php/comedica/article/view/556/949
55. Secretaría Nacional de Planificación y Desarrollo. (2009). Plan Nacional del Buen Vivir. Objetivo 3. Mejorar la calidad de vida de la población, 137-138. Quito, Ecuador. Recuperado de http://www.buenvivir.gob.ec/objetivo-3.-mejorar-la-calidad-de-vida-de-la-poblacion
56. Valenzuela, R., Bascuñán, K., Chamorro, R., Barrera, C., Sandoval, J., Puigrredon, C., et al. (2015). Modification of Docosahexaenoic Acid Composition of Milk from Nursing Women Who Received Alpha Linolenic Acid from Chia Oil during Gestation and Nursing. 7(8), 6405–6424. doi: 10.3390/nu7085289.
FINANCIACIÓN
Ninguna.
CONFLICTO DE INTERÉS
Ninguno.
CONTRIBUCIÓN DE AUTORÍA
Conceptualización: Francisca Patricia Jimenez Granizo, Glenda Marcela Sarmiento Tomalá, Zoraida Burbano Gómez, Alondra Idrovo Encalada, Pilar Asunción Soledispa Cañarte, Alexandra López Barrera.
Curación de datos: Francisca Patricia Jimenez Granizo, Glenda Marcela Sarmiento Tomalá, Zoraida Burbano Gómez, Alondra Idrovo Encalada, Pilar Asunción Soledispa Cañarte, Alexandra López Barrera.
Análisis formal: Francisca Patricia Jimenez Granizo, Glenda Marcela Sarmiento Tomalá, Zoraida Burbano Gómez, Alondra Idrovo Encalada, Pilar Asunción Soledispa Cañarte, Alexandra López Barrera.
Redacción – borrador original: Francisca Patricia Jimenez Granizo, Glenda Marcela Sarmiento Tomalá, Zoraida Burbano Gómez, Alondra Idrovo Encalada, Pilar Asunción Soledispa Cañarte, Alexandra López Barrera.
Redacción – revisión y edición: Francisca Patricia Jimenez Granizo, Glenda Marcela Sarmiento Tomalá, Zoraida Burbano Gómez, Alondra Idrovo Encalada, Pilar Asunción Soledispa Cañarte, Alexandra López Barrera.