doi: 10.56294/hl2023249
ORIGINAL
Evaluation of the hepatoprotective effect of extracts of brown seaweed Sargassum ecuadoreanum
Evaluación del efecto hepatoprotector presente en extractos de algas pardas Sargassum ecuadoreanum
Glenda Marcela Sarmiento Tomalá1 ![]() *, Zoraida Burbano Gómez1
*, Zoraida Burbano Gómez1 ![]() *, Pilar Asunción Soledispa Cañarte1
*, Pilar Asunción Soledispa Cañarte1 ![]() *, Alexandra López Barrera1
*, Alexandra López Barrera1 ![]() *, Francisca Patricia Jimenez Granizo1
*, Francisca Patricia Jimenez Granizo1 ![]() *, María Guadalupe
García Moncayo1
*, María Guadalupe
García Moncayo1 ![]() *
*
1Universidad de Guayaquil, Facultad de Ciencias Químicas. Guayaquil, Ecuador.
Citar como: Sarmiento Tomalá GM, Burbano Gómez Z, Soledispa Cañarte PA, López Barrera A, Jimenez Granizo FP, García Moncayo MG. Evaluation of the hepatoprotective effect of extracts of brown seaweed Sargassum ecuadoreanum. Health Leadership and Quality of Life. 2023; 2:249. https://doi.org/10.56294/hl2023249
Enviado: 29-04-2023 Revisado: 14-07-2023 Aceptado: 12-10-2023 Publicado: 13-10-2023
Editor:
PhD.
Prof. Neela Satheesh ![]()
Autor para la correspondencia: Glenda Marcela Sarmiento Tomalá *
ABSTRACT
This study consisted of evaluating the hepatoprotective effect present in the hydroalcoholic extract of brown algae (Sargassum ecuadoreanum) in mice. The collection was carried out on the beach Ballenita (Ecuador), chemical physical parameters were determined to the drug raw and the hydroalcoholic extract such as: Total ash, Water soluble ash, HCl insoluble ash, Total solids, Total fats, Humidity, Percentage of yield, total polysaccharides and sodium chloride. The induction was carried out with 5 % intraperitoneally carbon tetrachloride and the treatment lasted for seven days. Seven groups were formed: a normal control group without treatment and without induction, an untreated negative control group, groups treated with Silymarin (420 mg/kg) and N-acetylcysteine (600 mg/kg orally) orally plus induction and groups treated with the hydroalcoholic extract of the research model at doses of 1000 mg/kg, 500 mg/kg, 250 mg/kg orally plus induction. A histopathological study and a biochemical assay were conducted to determine levels of Oxalactic Glutamic Transaminase (TGO). As a result, the sample presented total polysaccharides concentrations, the groups treated with Silymarin, N- acetyl cysteine and the hydroalcoholic extract at different doses, were similar to the transaminase values (TGO) of the normal control group, while the negative control group showed significant difference of 0,05 %. Moreover, the histopathological study indicated that liver damage was in its first stage of injury, however, the hydroalcoholic extract of the brown seaweed Sargassum ecuadoreanum had a preventive hepatoprotective effect.
Keywords: Polysaccharides; Brown Algae; Hepatoprotective Activity; Liver Diseases; CCl4 Carbon Tetrachloride.
RESUMEN
Este estudio consistió en evaluar el efecto hepatoprotector presente en el extracto hidroalcohólico de algas pardas (Sargassum ecuadoreanum) en ratones. La recolección se llevó a cabo en la playa Ballenita (Ecuador), se determinaron parámetros físicos químicos a la droga cruda y al extracto hidroalcohólico como: Cenizas totales, Cenizas solubles en agua, Cenizas insolubles en HCl, Sólidos totales, Grasas totales, Humedad, Porcentaje de rendimiento, Polisacáridos totales y Cloruro de sodio. La inducción fue realizada con tetracloruro de carbono al 5 % por vía intraperitoneal y el tratamiento tuvo una duración de siete días. Se conformaron 7 grupos: un grupo control normal sin tratamiento y sin inducción, un grupo control negativo sin tratamiento, grupos tratados con silimarina (420 mg/kg) y N-acetilcisteína (600 mg/kg vía oral) por vía oral más inducción y grupos tratados con el extracto hidroalcohólico del modelo de investigación a dosis de 1000 mg/kg, 500 mg/kg, 250 mg/kg por vía oral más inducción. Se realizó un estudio histopatológico y un ensayo bioquímico para determinar niveles de transaminasa Glutámico Oxalacética (TGO). Como resultado, la muestra presentó concentraciones de polisacáridos totales, los grupos tratados con Silimarina, N- acetil cisteína y el extracto hidroalcohólico a diferentes dosis, tuvieron similitud a los valores de transaminasa (TGO) del grupo control normal, mientras que, el grupo control negativo mostró diferencia significativa del 0,05 %. Por otra parte, el estudio histopatológico indicó que el daño hepático estaba en su primera fase de estadios, sin embargo, el extracto hidroalcohólico del alga parda Sargassum ecuadoreanum presentó un efecto hepatoprotector preventivo.
Palabras clave: Polisacáridos; Algas Pardas; Actividad Hepatoprotectora; Enfermedades Hepáticas; Tetracloruro de Carbono CCl4.
INTRODUCCIÓN
En países de Asia Oriental se ha evidenciado el estudio de diversos géneros y especies de las algas marinas como una fuente alimenticia y nutricional gracias a su aporte de vitaminas y minerales, además sobre diversos efectos beneficiosos para la salud.
Las algas pardas del género Sargassum producen metabolitos secundarios con un alto potencial de actividades biológicas entre ellas terapéuticas y farmacológicas, estas sustancias bioactivas son: polisácaridos, terpenoides, oxilipinas, florotaninos, hidrocarburos volátiles entre otros, las funciones de estos determinados compuestos tienen la capacidad de actuar como antioxidante, antimicrobianos, inhibidores de diferentes enzimas y hepatoprotectores.(1)
Las enfermedades hepáticas muchas veces se originan por factores hereditarios, por el exceso o mal uso de fármacos y abuso de sustancias alcohólicas, dichas causas provocan lesiones y degeneraciones al tejido hepático ocasionando un déficit en el funcionamiento celular de este órgano.
En Ecuador existe una gran diversidad de algas entre ellas las pardas, sin embargo existen fuentes con escasa información y evidencia científica relevante que indique que las algas pardas del género Sargassum poseen actividad hepatoprotectora, por ello en el presente trabajo de investigación experimental, se pretende evaluar el efecto hepatoprotector presente en extractos de algas pardas Sargassum ecuadoreanum sobre el daño hepático inducido por tetracloruro de carbono en ratones de experimentación.
Objetivo general
Evaluar el efecto hepatoprotector que presenta el extracto hidroalcohólico de algas pardas (Sargassum ecuadoreanum) en animales de experimentación.
MÉTODO
Variables de la investigación
Variable dependiente
Propiedades fisicoquímicas de la droga cruda: Humedad, cenizas, grasas, sólidos totales, polisacáridos totales, Cloruro de sodio (ClNa).
Propiedades fisicoquímicas del extracto hidroalcohólico: pH, densidad, contenido de ClNa, sólidos totales.
Variable independiente
Ensayos de control de calidad a la droga cruda.
Extracto hidroalcohólico.
Estudio histopatológico.
Estudio bioquímico de transaminasas (TGO).
Dosis.
Operacionalización de las variables


Figura 1. Definición operacional de las variables
El presente estudio consta de un diseño experimental de carácter cuantitativo, al emplear variables que fueron manipuladas como: dosificación del extracto hidroalcohólico del alga parda Sargassum ecuadoreanum, parámetros de control de calidad en la droga cruda y extracto. A su vez, la realización de ensayos in vivo con biomodelos de experimentación con el fin de establecer grupos de control y grupos post prueba mediante un estudio histopatológico.
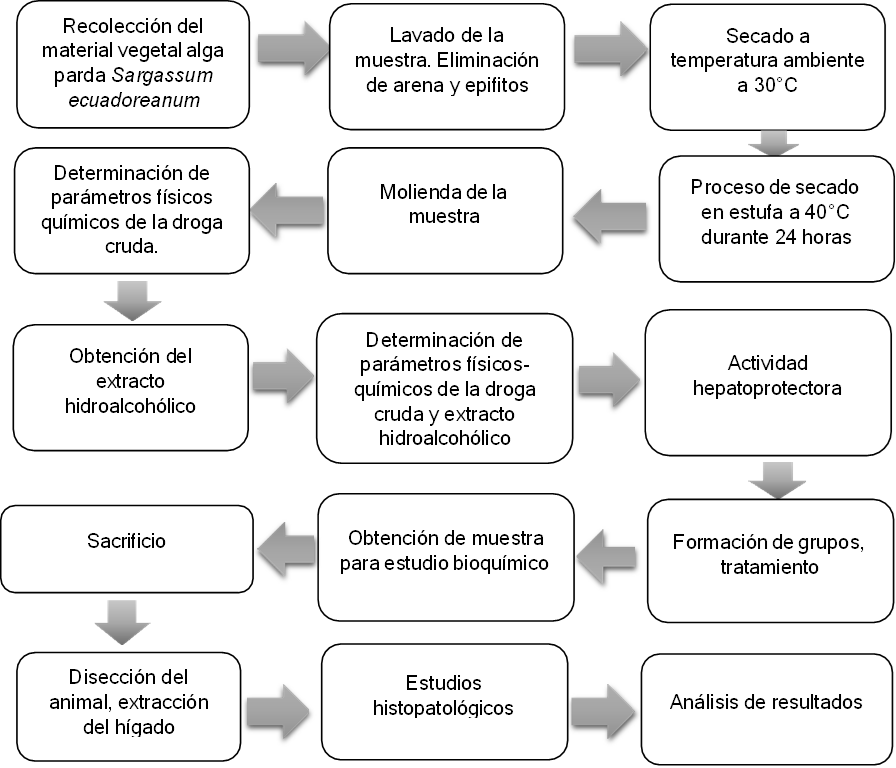
Figura 2. Diagrama de la metodología de la investigación
Materiales
· Vaso precipitado.
· Piseta.
· Agitador de vidrio.
· Capilares.
· Tubos eppendorf.
· Crisol de porcelana.
· Papel filtro libre de cenizas.
· Matraz aforado.
· Vidrio de reloj.
· Probeta.
· Embudo.
· Desecador de vidrio.
· Bureta de 50 ml.
· Tirillas reactivas ph.
· Frasco de vidrio ámbar.
· Cánula.
· Jeringuillas (de insulina).
· Tubos activadores de coágulos séricos en suero alto a gran altitud de 5 ml (cat serum sep clot activator high altitude 5 ml.
Reactivos
· n-Hexano.
· Ácido clorhídrico al 10 %.
· Etanol al 92 %.
· Fenol.
· ácido sulfúrico concentrado.
· Nitrato de plata 0,1 mol/L.
· Cloruro de sodio.
· Bicarbonato de sodio.
· Cromato de potasio.
· Agua destilada.
· Tetracloruro de carbono al 5 %.
· Formaldehido al 37 %.
· Aceite de oliva.
· Silimarina 140 mg.
· N- acetil cisteína 600 mg.
· Éter etílico.
Equipos
· Agitador magnético.
· Estufa.
· Hornilla eléctrica.
· Horno mufla.
· Equipo espectrofotométrico.
· Genesys 20 (Serie 4804640).
· Balanza analítica.
· Balanza para pesaje de animales pequeños.
· Refrigerador.
· Sorbona.
Diseño experimental de la investigación
Recolección del material vegetal
Para la realización del presente estudio se procedió a recolectar el material algal en la península de Santa Elena (Ecuador) durante las horas de baja marea en áreas rocosas de la zona intermareal correspondiente a la playa Ballenita (Balneario).
La recolecta de las plantas marinas se realizó en el mes de julio del presente año de forma manual para luego ser pesadas, almacenadas a baja temperatura y transportada al laboratorio de la facultad de Ciencias Químicas. Una parte de ella fue enviada a la facultad de Ciencias Naturales para ser clasificadas taxonómicamente.
Preparación y secado de las algas pardas Sargassum ecuadoreanum
Fueron sometidas a una limpieza manual con abundante agua corriente y enjuagadas con agua destilada para eliminar restos de arena y epifitos. Las algas se secaron durante 48 horas a temperatura ambiente y posterior a 24 horas en una estufa a 40°C, finalmente se trituraron mediante el empleo de un molinillo eléctrico hasta obtener un polvo fino y ser conservadas en envases herméticos.
Para ello, el polvo obtenido tuvo que someterse a controles físico-químicos para ser evaluada la calidad de la muestra y a continuación la obtención de los extractos.
Determinación de parámetros fisicoquímicos realizados en las algas pardas Sargassum ecuadoreanum (droga cruda)
Determinación de Cenizas totales
Se pesó 2 gramos del material algal pulverizado en un crisol de porcelana o platino previamente tarado (A, B y C). Luego se incineró a una temperatura de 500-750°C por 3 horas en la mufla. Transcurrido el tiempo se retiraron las cenizas y se dejó enfriar en un desecador y se registró el peso de cada una de la replicas (A, B y C). Posteriormente se incineró nuevamente las cenizas por 2 horas repitiendo el proceso anterior, el residuo obtenido es de color blanco o casi blanco.
Se realizaron cálculos mediante la siguiente expresión de los resultados:
m2-m
CT= x100
m1-m
Donde
m2= Crisol con cenizas después de incineracion
m1= Crisol con muestra antes de incineración
m= Crisol vacío
CT= Cenizas totales
Grasas totales
Este análisis se llevó a cabo por el método de Folch. Se pesó 2 gramos de muestra de alga parda Sargassum ecuadoreanum en tubos de eppendorf. Luego se añadió 20 ml de n-hexano a cada tubo (A, B, C) se tapó y agito correspondientemente. Posteriormente se trasladaron los tubos a baño maría a una temperatura de 40°C por 10 minutos. Se dejó enfriar hasta que el polvo asiente, luego se procedió a separar el líquido sobrenadante del residuo y fue trasvasado a un beacker. Consecutivamente, se llevó el beacker que contiene el líquido sobrenadante a la estufa a una temperatura de 60°C para eliminar el n- hexano. Finalmente se pesó y se obtuvo por diferencia el porcentaje de grasas contenido en la muestra.
Se realizaron los cálculos mediante la siguiente expresión de los resultados:

Determinación de Cenizas solubles en agua
A las cenizas totales obtenidas, se les añadió de 15 a 20 ml de agua destilada. El crisol se tapó y se sometió a ebullición suavemente a la llama de un mechero durante 5 minutos. Se filtró la solución a través de un papel filtro libre de cenizas. El filtro con el residuo se transfirió al crisol inicial, se carbonizó en un mechero y luego se incineró en un horno mufla a una temperatura de 700-750 °C durante 2 horas. Posteriormente se colocó en una desecadora y cuando este alcanzó la temperatura ambiente se pesó. El procedimiento se repitió hasta alcanzar peso constante.
Expresión de resultados
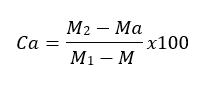
Donde
M2= Masa del crisol con las cenizas totales (g).
M1= Masa del crisol con la muestra de ensayo (g).
Ma= Masa del crisol con las cenizas insolubles en agua.
Ca= Porcentaje de cenizas solubles en agua en base hidratada.
M= Masa del crisol vacío.
100= Factor matemático.
Cuantificación de polisacáridos (preparación de la muestra)
Por triplicado, se pesó 2 gramos de muestra y fue transferida a un matraz aforado de 500 ml y se añadió 100 ml de etanol al 92 %, se llevó a reflujo por una hora y se filtró en caliente. El residuo del papel fue transferido nuevamente en el matraz aforado y se añadió 100 ml de agua destilada, se llevó a reflujo por 2 horas y se filtró en caliente en matraces de 200 ml, posteriormente se procedió a enfriar y enrasar.
Se tomó una alícuota de 0,25 ml a cada réplica y se transfirió a tubos eppendorf y se añadió 750 ul de agua destilada, 1 ml de fenol y 4 ml de ácido sulfúrico concentrado (H2SO4). Se dejó en reposo por 10 minutos y se transfirió a baño maría por 15 minutos a una temperatura de 40°C. Posteriormente se procedió a leer en un espectrofotómetro Genesys 20 EQ-24 (serie 4804640).
Cuantificación de polisacáridos (preparación de los estándares)
Para este análisis se pesó 51 mg de glucosa anhidra en un vidrio de reloj y se transfirió a un matraz volumétrico de 50 ml y se enrasó con agua destilada. Se procedió a tomar una alícuota de 2 ml y fue transferida a un matraz volumétrico de 25 ml. Se tomó de la solución diferentes alícuotas de: 1 ml - 0,75 ml - 0,50 ml - 0,25 ml y fueron trasvasados a tubos eppendorf en donde se añadió a cada tubo 1 ml de fenol al 5 % y 4 ml de ácido sulfúrico concentrado. Luego se dejó en reposo por 10 minutos y se llevó a baño maría por 15 minutos a una temperatura de 40°C. Para la preparación del blanco se requirió 1 ml de agua destilada, 1 ml de fenol al 5 % y 4 ml de ácido sulfúrico. Posteriormente se leyeron absorbancias en un espectrofotómetro Genesys 20 EQ-24 (serie 4804640) cada una de las concentraciones preparadas y el blanco.
Determinación de cenizas insolubles en ácido clorhídrico
A las cenizas totales obtenidas, se les añadió de 2-3 ml de ácido clorhídrico al 10 %. El crisol se tapó con un vidrio reloj y se calentó sobre un baño de agua hirviente durante 10 min. Se lavó el vidrio reloj con 5 ml de agua caliente y se unió al contenido del crisol. La solución se filtró a través de papel filtro libre de cenizas; se lavó el residuo con agua caliente hasta que el filtrado acidulado con ácido clorhídrico al cual se le agregó una a dos gotas de solución de nitrato de plata 0,1 mol/L, hasta que este no muestre presencia de cloruros.
El filtrado con el residuo fue desecado a una temperatura de 100 a 105°C, se transfirió al crisol inicial y se procedió a incinerar en un horno mufla a una temperatura de 700-750°C durante 2 horas. Posteriormente se colocó en una desecadora y cuando se alcanzó la temperatura ambiente se pesó correspondientemente. Este procedimiento se repitió hasta obtener masa constante.
Expresión de resultados
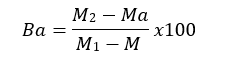
Donde
M2= Masa del crisol con las cenizas totales (g).
M1= Masa del crisol con la muestra de ensayo (g).
Ma= Masa del crisol con las cenizas insolubles en agua.
Ca= Porcentaje de cenizas solubles en agua en base hidratada.
M= Masa del crisol vacío.
100= Factor matemático.
Determinación de sodio contenido en la droga cruda por Absorción Atómica
Este análisis fue realizado por laboratorios UBA, donde se solicitó 100 gramos de la muestra para posterior análisis por el método AOAC 965.09 (Absorción Atómica).
Determinación de parámetros fisicoquímicos realizados al extracto hidroalcohólico de algas pardas Sargassum ecuadoreanum
Preparación del extracto hidroalcohólico al 20 %
Para la preparación del solvente se procedió a medir en una probeta 70 ml agua destilada libre de cloruros y 30 ml de etanol al 92 %. Luego se pesó 20 gramos del polvo, es decir la droga cruda y fue transferida a un beacker, y posteriormente se añadieron los 100 ml del solvente con agitación constante y se dejó macerar por 24 horas. Transcurrido el tiempo de maceración, se procedió a separar el líquido sobrenadante y se filtró en una probeta e inmediatamente se midió el líquido macerado y se registró el volumen.
Finalmente, el líquido macerado fue trasvasado a un beacker y se llevó a baño maría a una temperatura de 100 °C por un tiempo aproximado de 2 horas con agitación constante hasta que desista el olor a etanol para la obtención del extracto.
Porcentaje de rendimiento del extracto hidroalcohólico
El cálculo del porcentaje de rendimiento consiste en el volumen obtenido antes (rendimiento teórico) y después de la evaporación (rendimiento práctico), y está dado mediante la siguiente ecuación:

Determinación de pH en el extracto hidroalcohólico
Se añadió en una cápsula de vidrio cantidad suficiente del extracto y en ella se sumergió una tirilla reactiva, posteriormente se esperó de 5 a 8 minutos para registrar el valor según el grado de acidez o basicidad de la muestra.
Sólidos totales
Por triplicado, se pesaron cápsulas de vidrio vacías, y posteriormente se midió 5 ml del extracto y se añadió en las respectivas cápsulas. Finalmente se procedió a secar en una hornilla eléctrica y se introdujo el extracto en la estufa a una temperatura de 100 – 105°C por 2 horas.
Densidad
Por triplicado, se seleccionaron tres probetas de 10 ml y se registró el peso de cada una, luego se midió 10 ml del extracto en las respectivas probetas y se pesó con el contenido. Para calcular la densidad se empleó la siguiente ecuación:

Determinación de cloruro de sodio (ClNa) por titulación III.6.4.5.1 Preparación de la sustancia patrón tipo primario (ClNa)
Se pesó 58,44 mg de cloruro de sodio en un beacker, cabe recalcar que la sustancia patrón debe secarse en una estufa a una temperatura de 120°C por 2 horas. Se añadió la sustancia en un matraz de 50 ml y finalmente se enrasó el volumen.
Preparación de la sustancia titulante Nitrato de plata (NO3Ag)
Se pesó 4,25 g de nitrato de plata y se disolvió hasta enrasar en un matraz de 250 ml. Para la valoración del nitrato de plata, se transfirió la solución a una bureta de 50 ml y se dejó caer gota a gota en un beacker que contiene los 50 ml de la sustancia patrón tipo primario (ClNa) y el indicador ( CrO4K2 ) 2 a 3 gotas en constante movimiento con la ayuda de un agitador magnético, una coloración amarilla más un precipitado de color rojo ladrillo indican la presencia del cromato de plata. Se realizó 3 determinaciones.
Titulación de la muestra
La muestra debe tener un pH entre 7 – 9, y para ello se modificó a pH neutro. Se midió 2 ml del extracto, se diluyó y enrasó en un matraz de 50 ml, luego se transfirió la solución a un beacker de 100 ml y se añadió de 2 a 3 gotas del indicador cromato de potasio ( CrO4K2), cargada la bureta de 50 ml con la solución de nitrato de plata se dejó caer gota a gota con agitación constante a la solución muestra hasta observar la formación de un precipitado rojo ladrillo (cromato de plata).
Actividad Hepatoprotectora
Se utilizaron como reactivos biológicos ratones CD provenientes del Instituto Nacional de Salud pública e Investigación (INSPI), con un peso promedio de 25.
± 5 g cumpliendo con las buenas prácticas del cuidado y manejo de animales de experimentación, los cuales, fueron alimentados con abundante agua y balanceado dividiéndose en 7 grupos (cada grupo con 7 biomodelos) después de haber transcurrido 1 semana de aclimatación.
La división se la realizó de la siguiente manera: Un grupo control normal, un control positivo tratado con Silimarina a una dosis de 420 mg/kg, un grupo control positivo tratado con N-acetil cisteína a una dosis de 600 mg/kg (vía oral), un grupo control negativo en donde se realizó una inducción de daño hepático con tetracloruro de carbono (𝐶𝐶𝑙4), a una concentración del 5 % fijado con aceite de oliva por vía intraperitoneal. A demás, tres grupos fueron tratados con extracto hidroalcohólico de alga parda Sargassum ecuadoreanum a una dosis 1000 mg/kg, 500 mg/kg y 250 mg/Kg por vía oral, el pH del extracto tuvo que modularse con bicarbonato de sodio a neutro (7) debido a que éste tenía un pH ácido (5).
El tratamiento duró 7 días, al sexto día se administró por vía intraperitoneal el tetracloruro de carbono (0,2 ml/kg) a los siguientes grupos: control positivo tratado con Silimarina a una dosis de 420 mg/kg, control positivo tratado con N- acetil cisteína a una dosis de 600 mg/kg, y a los tres grupos tratados con el extracto hidroalcohólico de alga parda Sargassum ecuadoreanum (dosis 1000 mg/kg, 500 mg/kg y 250 mg/Kg), y se continuó con el tratamiento hasta el séptimo día, posteriormente se anestesiaron a 20 modelos biológicos (escogidos entre los siete grupos) con éter y se realizó una toma de muestra sanguínea de aproximadamente 1 ml por vía ocular para el respectivo análisis bioquímico de Transaminasa Glutámico Oxalacética (TGO) cuya muestra fue recogida en tubos activadores de coágulos séricos en suero alto a gran altitud de 5 ml (CAT Serum Sep Clot Activator High Altitude 5 ml), posteriormente los reactivos biológicos fueron sacrificados mediante previa anestesia y luego dislocación cervical y se realizó una disección para extraer el hígado y posterior análisis histopatológico. Los resultados fueron analizados estadísticamente.
Determinación de los parámetros físicos químicos
Cenizas
Como lo muestra en la tabla 2 se calculó el promedio, desviación estándar y coeficiente de variación (1,9 %) de las dos replicas B y C descartándose la réplica A porque incidía en los valores de las dos replicas anteriormente mencionadas.
|
Tabla 2. Promedio del porcentaje de cenizas totales contenidos en la droga cruda |
|
|
Réplicas |
Porcentaje de Cenizas |
|
B |
14,93 |
|
C |
14,52 |
|
Promedio |
14,72 ± 0,29 |
Grasas
La tabla 3 muestra el promedio del porcentaje de grasas totales contenidas en la droga cruda, además de la desviación estándar y el coeficiente de variación (6,896 %)
|
Tabla 3. Promedio del porcentaje de grasas totales contenidas en la droga cruda |
|
|
Porcentaje de grasas totales |
|
|
A |
0,80 |
|
B |
0,91 |
|
C |
0,90 |
|
Promedio |
0,87 ± 0,060 |
Cenizas solubles en agua
En la tabla 4 se muestra el promedio del porcentaje de cenizas totales solubles en agua y desviación estándar, en esta determinación se descartó la réplica A porque incidía en las dos replicas siguientes (B y C), el coeficiente de variación es de 3,5 %.
|
Tabla 4. Promedio del porcentaje de cenizas solubles en agua contenidas en la droga cruda |
|
|
Réplica |
Porcentaje de cenizas solubles en agua |
|
B |
9,458 |
|
C |
9,951 |
|
Promedio |
9,70 ± 0,348 |
Determinación de sodio por absorción atómica
Este análisis fue realizado por laboratorios UBA, según la AOAC 965.09 absorción atómica, indica un valor del 0,70 % de sodio como lo muestra a continuación la tabla 5.
|
Tabla 5. Resultado de análisis para la determinación de sodio contenido en la droga cruda por absorción atómica |
|||||
|
Código UBA |
Parámetros |
Método |
Resultados |
Unidad |
Límite de cuantificación |
|
UBA- 26796-1 |
Sodio (Na) |
AOAC 965.09 (Absorción Atómica) |
0,70 |
% |
- - |
Polisacáridos totales
En la figura 3 se muestra la curva de calibración de polisacáridos totales, teniendo un R² = 0,9866 cuyo valor permitió calcular la concentración de polisacáridos contenidos en la droga cruda.
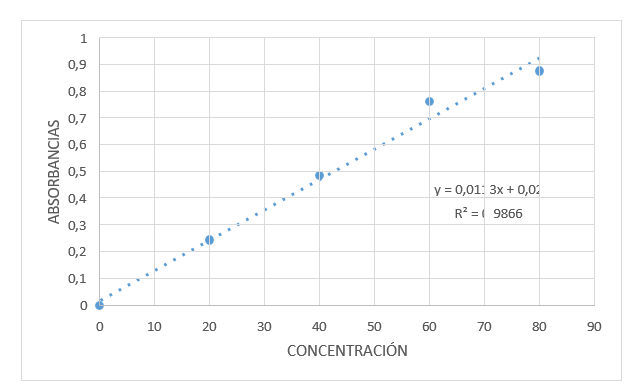
Figura 3. Curva de calibración de polisacáridos totales contenidos en la droga cruda
A continuación, en la tabla 6 se obtuvo el promedio de la concentración de polisacáridos totales contenidos en la droga cruda, la desviación estándar y el coeficiente de variación cuyo valor es de 7,8 %, se descartó la réplica A porque incidía en las dos siguientes.
|
Tabla 6. Promedio de la concentración de polisacáridos totales contenidos en la droga cruda |
|
|
Réplica |
Concentración de la muestra |
|
B |
108,63 ug/g |
|
C |
97,22 ug/g |
|
Promedio |
102,92 ± 8,06 |
Cenizas insolubles en acido clorhidrico (HCI)
A continuación, en la tabla 7 obtuvo finalmente el promedio de cenizas insolubles en ácido clorhídrico, desviación estándar y coeficiente de variación cuyo valor es de 0,078 %.
|
Tabla 7. Promedio del porcentaje de cenizas insolubles en ácido clorhídrico (HCl) contenidas en la droga cruda |
|
|
Réplica |
Porcentaje de cenizas insolubles en HCl |
|
A |
97,862 |
|
B |
97,730 |
|
C |
97,866 |
|
Promedio |
97,819 ± 0,077 |
Determinación de parámetros fisicoquímicos realizados en el extracto hidroalcohólico de algas pardas Sargassum ecuadoreanum
Determinación del porcentaje de rendimiento, densidad, humedad y solidos totales
A continuación, en la tabla 8 se observan los resultados obtenidos de los parámetros realizados al extracto, tales como: porcentaje de rendimiento, promedio de la densidad, promedio del porcentaje de solidos totales con una desviación estándar del 1,37 %, y porcentaje de humedad.
|
Tabla 8. Porcentaje de rendimiento, porcentaje de humedad, promedio del porcentaje de solidos totales y promedio de la densidad del extracto hidroalcohólico |
|||
|
Porcentaje de rendimiento del extracto |
Porcentaje de humedad |
Promedio de la densidad del extracto |
Promedio del porcentaje de solidos totales |
|
63,2 % |
94,9 % |
0,995 ± 0,004 |
5,1± 0,07 |
Valoración del cloruro de sodio
Para la titulación de la sustancia patrón, como se muestra en la Tabla 9 se obtuvo el promedio del porcentaje del mismo, desviación estándar y coeficiente de variación cuyo valor es de 3,5 %.
|
Tabla 9. Promedio del porcentaje de la valoración de la sustancia patrón tipo primario cloruro de sodio (NaCl) |
|
|
Réplicas |
Normalidad (g/L) |
|
A |
0,101 |
|
B |
0,095 |
|
C |
0,095 |
|
Promedio |
0,097 ± 0,0034 |
Valoración del extracto hidroalcohólico
Se define que por cada 100 ml de extracto hay un 2 % de cloruro de sodio contenido en la muestra; como se observa a continuación en la tabla 10 se obtuvo el promedio, desviación estándar y coeficiente de variación, cuyo valor es de 2,99 %.
|
Tabla 11. Promedio del porcentaje de cloruro de sodio contenido en el extracto hidroalcohólico del alga parda Sargassum ecuadoreanum |
|
|
Réplicas |
Porcentaje de la muestra |
|
A |
2,454 % |
|
B |
2,331 % |
|
C |
2,331 % |
|
Promedio |
2,37 ± 0,071 |
Pruebas bioquímicas: Transaminasa Glutámico Oxalacética (TGO)
En el figura 4 que se muestra a continuación, se halla el promedio de los valores obtenidos de transaminasas TGO, de cada grupo de ensayo tratado.
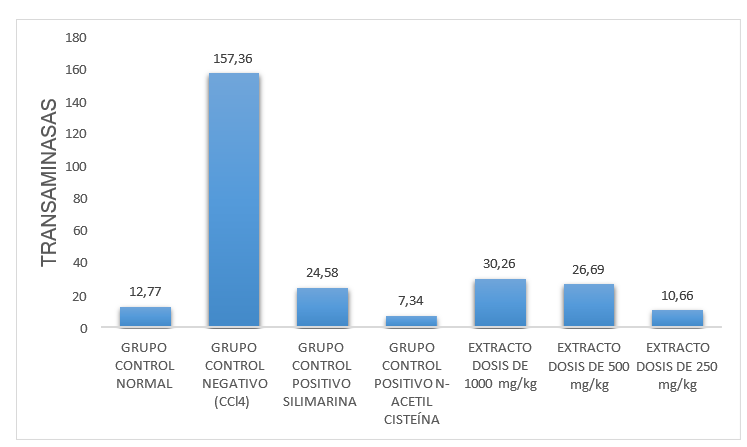
Figura 4. Promedios de transaminasa Glutámico Oxalacética TGO en la evaluación hepatoprotectora en ratones
De acuerdo al resultado del análisis bioquímico de transaminasa glutámico oxalacética (TGO), los grupos tratados con Silimarina (24,58 ± 25,18), N- acetil cisteína (7,34 ± 4,31) y el extracto hidroalcohólico con sus respectivas dosificaciones (dosis 1000 mg/kg: 30,26 ± 24,22, dosis 500 mg/kg: 26,69 ± 26,86, dosis 250 mg/kg: 10,66 ± 3,19), tuvieron similitud a los valores de transaminasa del grupo control normal (12,77 ± 0,90) , sin embargo, en relación con el grupo control negativo con CCL4 ( 157,36 ± 25,33) mostró diferencia con todos los grupos tratados ya mencionados anteriormente, por lo que estadísticamente presentó una diferencia significativa con una probabilidad del 0,05 %.
RESULTADOS
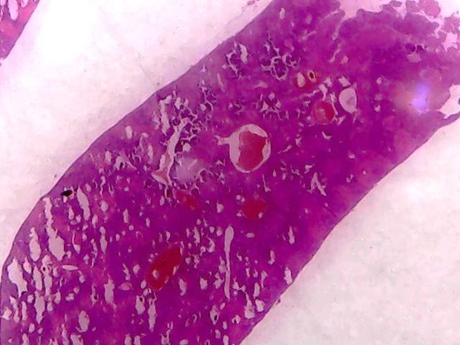
Resultado histopatológico del Hígado (Tinción hematoxilina-eosina)

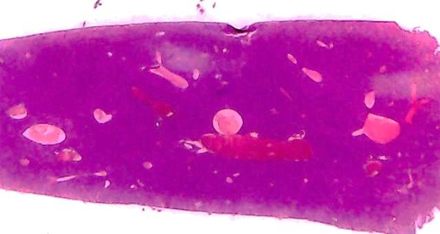
Figura 5. Grupo 1 Control normal sin tratamiento, sin inducción
Un órgano presentó leve metamorfosis grasa (degeneración) alrededor de los lobulillos, y discreta congestión portal.
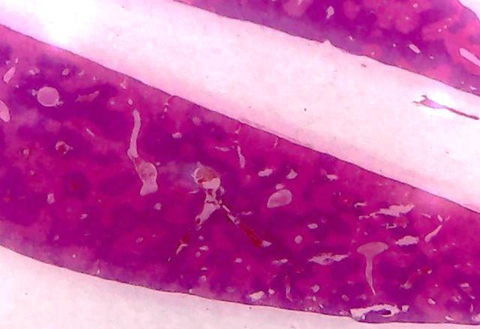
Figura 6. Grupo 2 control negativo tetracloruro de carbono CCL4 sin tratamiento
En todos los órganos se observó marcada degeneración turbia (+++) y a veces degeneración grasa +, todo ello perilobulillar, además una congestión portal y parenquimal (+), en un órgano se observa pequeños focos necróticos celulares (+).
Figura 7. Grupo 3 control positivo Silimarina + CCL 4
El grado de turbidez (degeneración) perilobulillar es recurrente en todos los órganos (++), la congestión vascular portal y parenquimal esta aumentada. (++).
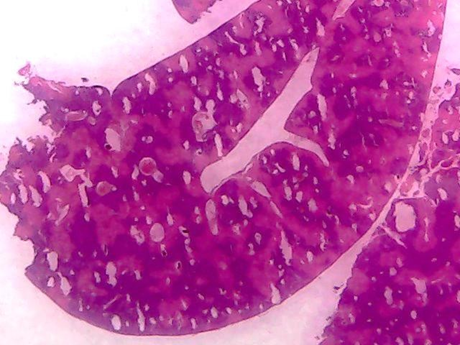
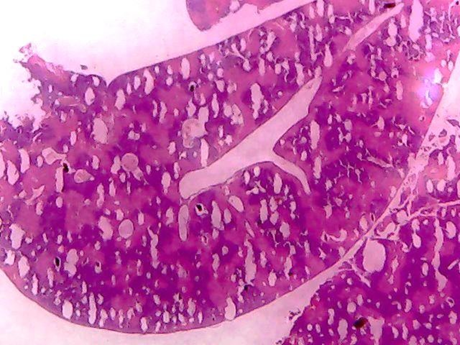
Figura 8. Grupo 4 Control positivo N – Acetil cisteína + CCL4
Al igual que en los casos anteriores la degeneración turbia perilobuliliar (presencia de pseudolobulillos) y la observación en un órgano de focos necróticos dispersos es evidente (+++), igualmente la congestión vascular esta manifiesta (++).

Figura 9. Grupo 5 Dosis 1000 mg/Kg Extracto + CCL4
El grado de turbidez celular (degeneración) perilobuliliar es discreta (++) pero manifiesta.

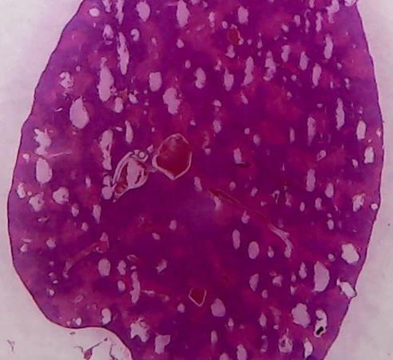
Figura 10. Grupo 6 Dosis 500 mg/kg, Extracto + CCL4
En un hígado aparece un amplio campo de necrosis subcapsular como respuesta evidente del proceso de degeneración turbia perilobuliliar (+++), los otros órganos presentan el mismo cuadro, pero en menor grado (++).
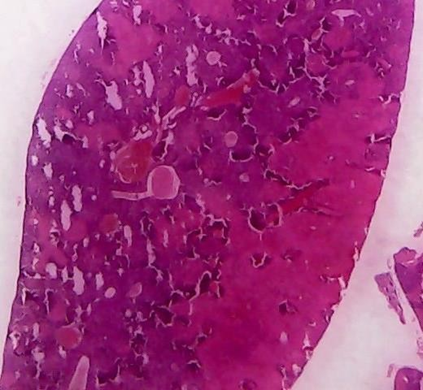

Figura 11. Muestra dosis 250 mg/kg Extracto + CCL4
Es similar el grado de degeneración turbia (++) a los anteriores, en un órgano está acompañado de una leve degeneración grasa (+).
DISCUSIÓN
Los datos obtenidos en el presente estudio preliminar mostraron una disminución de niveles de transaminasa glutámico oxalacética (TGO) a una dosis de 250 mg/kg (10,66 ± 3,19), dichos valores mantienen relación con los resultados del grupo control normal (12,77 ± 0,90) que, en este caso, no recibieron inducción de daño hepático con tetracloruro de carbono (CCL4) al 5 % por vía de administración intraperitoneal, ni tratamiento con el extracto hidroalcohólico. Además, estos valores se aproximan con el grupo control positivo tratado con N- acetil cisteína (7,34 ± 4,31) a una dosis de 600 mg/kg de peso por vía oral por un tiempo de siete días. Por otra parte, el grupo control negativo (157,36 ± 25,33) sin tratamiento fue el único que mantuvo valores elevados de la enzima sérica hepática TGO, el cual, sobrepasa los valores referenciales (97,63 ± 55,46). Los resultados actuales guardan similitud con los de Hira et al. (35) en el que administraron extractos etanólicos de Sargassum ilicifolium, S. laceolatum y S. swartzii a una dosis de 200 mg/kg de peso en ratas diariamente durante catorce días, comprobando que los extractos de S. ilicifolium y S. swartzii mantuvieron bajos los niveles de enzimas hepáticas después de la inducción con CCL4.(3,4,5,6,7,8,9,10)
En contraste, Quintal et al.(2) establecieron una dosis de 50 mg/kg de peso del extracto etanólico de Sargassum fluitans por vía de administración oral, el cual redujo marcadores enzimáticos en lesiones hepáticas agudas inducidas por acetaminofén y actividad hepatoprotectora en un modelo de daño crónico inducido con 𝐶𝐶𝑙4 en ratas en un periodo de doce semanas. El grupo control negativo también fue el único que mantuvo niveles elevados de transaminasas hepáticas (303,17 ± 38,61), en comparación a los grupos restantes.
Con respecto al tiempo de administración de los extractos de las especies Sargassum ya citados, coincidieron con la disminución de transaminasas TGO frente a los modelos inductores de daño hepático en diferentes periodos de tiempo con relación al presente estudio.(11,12,13,14,15,16,17,18)
No existe suficiente información referente al empleo de extractos hidroalcohólico en algas del género Sargassum. El objetivo de realizar un extracto hidroalcohólico en este trabajo, se debió a la afinidad que tienen algunos polisacáridos bioactivos con el alcohol, los cuales, son extraídos manteniéndose fijos en el sistema acuoso una vez evaporada la parte etanólica del solvente, por lo tanto, se lograron obtener resultados favorables a partir de este extracto en lo que corresponde al ensayo bioquímico de transaminasa TGO.(19,20,21,22,23,24,25) A pesar de que en varios estudios mencionados anteriormente utilizaron extractos diferentes, comprobaron actividad hepatoprotectora. Raghavendran et al.(36) informaron efectos hepatoprotectores a partir del extracto alcohólico de Sargassum polycystum al inhibir radicales libres generados durante la peroxidación lipídica en la hepatitis tóxica inducida por acetaminofén por lo que hubo una disminución significativa en la gravedad de la hepatitis tóxica.(26,27,28,29,30)
Los parámetros de control de calidad como grasas (0,28 %) humedad (85,1 %) y cenizas (30,52 %) obtenidos por Villegas(37) reflejan un alto contenido de material inorgánico y carbohidratos, y un bajo contenido de extracto etéreo en el alga parda Sargassum lapazeanum. Mientras que la especie Sargassum ecuadoreanum refleja un alto contenido de grasas (0,87 %), humedad (94,9 %), presencia de polisacáridos (102,92 ± 8,06) y un bajo contenido de material inorgánico (14,72 %) en comparación a la especie S. lapazeanum.
En los resultados de análisis histopatológico en relación con el grupo control negativo (CCl 4) se observó en todos los órganos marcada degeneración turbia y a veces degeneración grasa, todo ello perilobuliliar, además una congestión portal y parenquimal. A su vez, se observó en uno de los órganos pequeños focos necróticos celulares.(31,32,33,34,35,38,39) Con el grupo control tratado con Silimarina + CCl 4, el grado de turbidez (degeneración) perilobuliliar fue recurrente en todos los órganos aumentando la congestión vascular portal y parenquimal. Caso parecido ocurre con Quintal et al.(2) donde reporta que las secciones del grupo CCl 4 exhibieron células inflamatorias invasivas y pérdida de límites celulares, sin embargo, las secciones de los grupos Sil + CCl 4 y extracto etanólico de S. fluitans + CCl 4 tenían un patrón lobular generalmente normal con un grado leve de infiltración de linfocitos que estaba cerca del grupo de control, es decir, que el tratamiento con el extracto etanólico de S. fluitans evitó claramente cualquier lesión notable en los tejidos del hígado por la exposición a CCl 4. Por lo contrario, el tratamiento con el extracto hidroalcohólico de Sargassum ecuadoreanum a diferentes dosis, mostró que el daño hepático se encontraba en su primera fase de estadio debido al poco tiempo de tratamiento, y al uso de un agente altamente tóxico, de tal forma, no se obtuvieron los resultados deseados en la disminución del daño tisular.(40,41,42)
CONCLUSIONES
En el presente estudio se logró determinar los parámetros físico químicos que aseguran la eficacia tanto de la droga cruda como del extracto, señalando que el Sargassum ecuadoreanum está compuesto por un alto contenido de grasas, humedad, y bajo contenido de material inorgánico.
El material algal contiene concentraciones de polisacáridos totales que permitieron definir dosificaciones para comprobar la actividad biológica manifiesta en el extracto hidroalcohólico frente a un modelo de daño hepático.
Corroborando lo anterior, las dosis definidas del extracto regularon los niveles de TGO obteniéndose estadísticamente una diferencia significativa que farmacológicamente posee un efecto preventivo ante agresiones hepáticas.
Por otra parte, el estudio histopatológico indicó que el daño hepático se encontraba en su primera fase de estadio debido al poco tiempo de tratamiento, y al uso de un agente altamente hepatóxico, por lo que, no se obtuvieron los resultados deseados en la disminución del daño tisular.
REFERENCIAS BIBLIOGRÁFICAS
1. Yende S, Chaugule B, Harle U. Therapeutic potential and health benefits of Sargassum species. Pharmacogn Rev [Internet]. 2014 Jan [cited 2019 Jul 1];8(15):1. Available from: http://www.ncbi.nlm.nih.gov/pubmed/24600190
2. Quintal-Novelo C, Rangel-Méndez J, Ortiz-Tello Á, Graniel-Sabido M, Vaca RPC De, Moo-Puc R. A Sargassum fluitans Borgesen ethanol extract exhibits a hepatoprotective effect in vivo in acute and chronic liver damage models. Biomed Res Int. 2018;2018.
3. Asqui Lalón M de J. Actividad hepatoprotectora del extracto de diente de león (Taraxacum officinale) en ratas (Rattus norvegicus) con hepatotoxicidad inducida por tetracloruro de carbono [Tesis de Bachiller] [Internet]. 2012 [cited 2019 Oct 4]. Available from: http://dspace.espoch.edu.ec/handle/123456789/2590
4. Yende S, Harle U, Chaugule B. Therapeutic potential and health benefits of Sargassum species. Pharmacogn Rev. Wolters Kluwer--Medknow Publications; 2014;8:1–7.
5. Asanka Sanjeewa KK, Jayawardena TU, Kim HS, Kim SY, Shanura Fernando IP, Wang L, et al. Fucoidan isolated from Padina commersonii inhibits LPS-induced inflammation in macrophages blocking TLR/NF-κB signal pathway. Carbohydr Polym [Internet]. 2019 Nov 15 [cited 2020 Feb 18];224:115195. Available from: http://www.ncbi.nlm.nih.gov/pubmed/31472848
6. Echavarría BZ, Franco AS, Martínez AM. Evaluación de la actividad antioxidante y determinación del contenido de compuestos fenólicos en extractos de macroalgas del Caribe Colombiano. Vitae [Internet]. 2009 [cited 2020 Feb 18];16(1):126–31.
7. Chale-Dzul J, Pérez-Cabeza de Vaca R, Quintal-Novelo C, Olivera-Castillo L, Moo-Puc R. Hepatoprotective effect of a fucoidan extract from Sargassum fluitans Borgesen against CCl4-induced toxicity in rats. Int J Biol Macromol. 2020 Feb 15;145:500–9.
8. Namvar F, Mohamad R, Baharara J, Zafar-Balanejad S, Fargahi F, Rahman HS. Antioxidant, antiproliferative, and antiangiogenesis effects of polyphenol-rich seaweed (Sargassum muticum). Biomed Res Int. 2013;2013.
9. Solomon EP, Palacios Martínez R. Biología de Ville. McGraw-Hill Interamericana; 1998.
10. Mei X, Wu C, Zhao J, Yan T, Jiang P. Community structure of bacteria associated with drifting Sargassum horneri, the causative species of golden tide in the Yellow Sea. Front Microbiol [Internet]. 2019 May 28 [cited 2019 Jun 14];10:1192. Available from: http://www.ncbi.nlm.nih.gov/pubmed/31191503
11. Pastare L, Romagnoli F, Blumberga D. Comparison of biomethane potential lab tests for Latvian locally available algae. In: Energy Procedia. Elsevier Ltd; 2018. p. 277–81.
12. Basurto Broncano BK, Alcivár Mero KX. Determinación de las características fisicoquímicas del alga parda Sargassum ecuadoreanum en la zona intermareal, ubicada en Santa Elena [Internet]. 2019. Available from: http://www.ug.edu.ec/SitePages/historia.aspx
13. Gómez-Ordóñez E. Evaluación nutricional y propiedades biológicas de algas marinas comestibles. Estudios in vitro e in vivo. Tesis Doctoral. 2013.
14. Wang L, Oh JY, Hwang J, Ko JY, Jeon YJ, Ryu B. In vitro and in vivo antioxidant activities of polysaccharides isolated from celluclast-assisted extract of an edible brown seaweed, Sargassum fulvellum. Antioxidants. 2019 Oct 1;8(10).
15. Pozharitskaya ON, Shikov AN, Obluchinskaya ED, Vuorela H. The pharmacokinetics of fucoidan after topical application to rats. Mar Drugs [Internet]. 2019 Dec 6 [cited 2020 Feb 18];17(12):687. Available from:
16. van Weelden G, Bobi M, Okła K, van Weelden WJ, Romano A, Pijnenborg JMA. Fucoidan structure and activity in relation to anti-cancer mechanisms. Mar Drugs. 2019 Jan 7;17(1):32.
17. Sibulesky L. Normal liver anatomy. Clin Liver Dis. 2013;2(SUPPL. 1):2012–4.
18. Chumpitaz-Saravia VL, Villaverde-Saravia B, Vivanco-Hilario SD, Morales-García WC. Nursing care in a postoperative adnexal cystectomypatient in the Obstetrics and Gynecology Service of anational hospital in Chincha, 2023. Interamerican Journal of Health Sciences. 2023;4:169
19. Iza Toapanta MB. Determinación de daño hepático mediante TGO–TGP y fosfatasa alcalina en personal expuesto a plaguicidas en una empresa florícola de mayo a junio 2016. 2016;108. Available from: http://www.dspace.uce.edu.ec/handle/25000/8086
20. Zribi N, Boujelbène Y, Drerup MM, Waemustafa W, Sukri S, García-Marco T, et al. Efecto hepatoprotector del extracto acuoso de Ocimum basilicum L. “albahaca morada” en Rattus norvegicus variedad Sprague Dawley “ratas” intoxicados con tetracloruro de carbono Arequipa 2014. J Bank Financ [Internet]. 2015;5(1):643–54. Available from: http://dx.doi.org/10.1016/j.irfa.2010.03.001
21. Acosta Sero O, Rey MS, Spehrs E. Factors associated with weight loss trajectory in adults after sleeve gastrectomy. Interamerican Journal of Health Sciences. 2023;3:144
22. El-Kamary SS, Strickland GT. Hepatitis, Viral. In: International Encyclopedia of Public Health. Elsevier Inc.; 2016. p. 611–20.
23. Chen L, Zhang Q, Yu C, Wang F, Kong X. Functional roles of CCL5/RANTES in liver disease. Liver Res. 2020 Jan 28.
24. Méndez E, Orbe I, Parra V. Prevalencia, características de hepatopatías y factores asociados en el área de medicina interna del Hospital Vicente Corral Moscoso durante el periodo enero 2009 – diciembre 2010. 2010.
25. Lehninger, Mathews. Metabolismo de compuestos nitrogenados. 2010;20:2–3. Available from: http://www3.uah.es/bioquimica/Tejedor/bioquimica_quimica/R-T20-1-Rgenerales.pdf
26. Enst M, Anab R, Tez D, Dan LU, Yılmaz S, Baran Z, et al. Determinación de transaminasas (TGO y TGP) en los afiliados del Seguro Social Campesino-Dispensario Torata, que acuden a la Unidad de Atención Ambulatoria R-9 de Santa Rosa, 2014 [Internet]. Acta Universitatis Agriculturae et Silviculturae Mendelianae Brunensis. 2015;16:30–6. Available from: http://dx.doi.org/10.1080/14639947.2011.564813
27. Taleisnik S. Pruebas de función hepática. Rev Española Enfermedades Dig [Internet]. 2015 [cited 2019 Jul 3];40(3):73–8. Available from: http://scielo.isciii.es/scielo.php?script=sci_arttext&pid=S1130-01082015001000017
28. Lipovestky F, Radrizani D, Guantay E E, Casabella C, Lattanzio B, Casanova M, et al. Enteral bile reinfusion in severe abdominal trauma. Interamerican Journal of Health Sciences. 2023;3:15
29. Zhao SP, Wu ZS, Chen Y, Liang X, Bao L, Li P, et al. Protective effect of Hua Tan Qu Shi decoction against liver injury in rats with nonalcoholic fatty liver disease. Biomed Pharmacother [Internet]. 2017 Jul 1 [cited 2020 Feb 18];91:181–90. Available from: http://www.ncbi.nlm.nih.gov/pubmed/28458156
30. A GB, Daza EF, Juan EF, Parciales E, Tizzano EF. Hígado. Med y Lab. 2008;14(11–12):2009–2009.
31. Tejada F. Hepatotoxicidad por fármacos. Rev Clínica Med Fam. 2010;3(3):177–91.
32. Olivera Fuentealba Germán Alonso. Estudio del efecto protector y/o regenerador del aceite de Emú (Dromiceius oil) sobre el daño celular agudo inducido por tetracloruro de carbono en células hepáticas de ratas [Internet]. 2008. Available from: http://cybertesis.uach.cl/tesis/uach/2008/fco.48e/doc/fco.48e.pdf
33. Bolonia C De, Filippini F, Estudios C De. Universidad Complutense de Madrid 1-. 2011;1–16.
34. Mossanen JC, Tacke F. Acetaminophen-induced acute liver injury in mice. Lab Anim [Internet]. 2015 Apr 2 [cited 2020 Feb 18];49(1 Suppl):30–6. Available from: http://www.ncbi.nlm.nih.gov/pubmed/25835736
35. Sohrabinezhad Z, Dastan D, Asl SS, Nili-Ahmadabadi A. Allium Jesdianum extract improves acetaminophen-induced hepatic failure through inhibition of oxidative/nitrosative stress. J Pharmacopuncture. 2019;22(4):239.
36. Federico A, Dallio M, Loguercio C. Silymarin/Silybin and chronic liver disease: A marriage of many years. Molecules. 2017 Feb 1;22(2):191.
37. Kazemifar A, Kazemifar AM, Hajaghamohammadi AA, Samimi R, Alavi Z, Abbasi E, et al. Hepatoprotective property of oral silymarin is comparable to N-acetyl cysteine in acetaminophen poisoning. Gastroenterol Res [Internet]. 2012 Oct 31 [cited 2020 Feb 18];5(5):190–4. Available from: https://www.gastrores.org/index.php/Gastrores/article/view/495
38. Topón Jiménez ML, Lizcano-Ramirez JA, Morales-García WC. Educational interventions to combat anemia in pregnant women: nursing perspective. Interamerican Journal of Health Sciences. 2023;3:153.
39. Hira K, Sultana V, Ara J, Haque SE. Protective role of Sargassum species in liver and kidney dysfunctions and associated disorders in rats intoxicated with carbon tetrachloride and acetaminophen. Pak J Pharm Sci [Internet]. 2017 May [cited 2020 Mar 5];30(3):721–8. Available from: http://www.ncbi.nlm.nih.gov/pubmed/28653915
40. Balaji Raghavendran HR, Sathivel A, Devaki T. Antioxidant effect of Sargassum polycystum (Phaeophyceae) against acetaminophen-induced changes in hepatic mitochondrial enzymes during toxic hepatitis. Chemosphere. 2005 Oct 1;61(2):276–81.
41. Santos Rivera AL, Leones Cedeño AF, Chávez Arizala JF, Morales-García WC. Knowledge and practices on anemia in representatives of children under 5 years of age from the “Luz y Libertad” Educational Unit in La Concordia, 2023. Interamerican Journal of Health Sciences . 2023;3:170.
42. Villegas Silva VA. Evaluación del potencial de Sargassum lapazeanum Setchell & N.L. Gardner (Ochrophyta: Fucales, Phaeophyceae) como fuente de compuestos antibacterianos, antioxidantes y anticoagulantes. 2014.
FINANCIACIÓN
Ninguna.
CONFLICTO DE INTERÉS
Ninguno.
CONTRIBUCIÓN DE AUTORÍA
Conceptualización: Glenda Marcela Sarmiento Tomalá, Zoraida Burbano Gómez, Pilar Asunción Soledispa Cañarte, Alexandra López Barrera, Francisca Patricia Jimenez Granizo, María Guadalupe García Moncayo.
Curación de datos: Glenda Marcela Sarmiento Tomalá, Zoraida Burbano Gómez, Pilar Asunción Soledispa Cañarte, Alexandra López Barrera, Francisca Patricia Jimenez Granizo, María Guadalupe García Moncayo.
Análisis formal: Glenda Marcela Sarmiento Tomalá, Zoraida Burbano Gómez, Pilar Asunción Soledispa Cañarte, Alexandra López Barrera, Francisca Patricia Jimenez Granizo, María Guadalupe García Moncayo.
Redacción – borrador original: Glenda Marcela Sarmiento Tomalá, Zoraida Burbano Gómez, Pilar Asunción Soledispa Cañarte, Alexandra López Barrera, Francisca Patricia Jimenez Granizo, María Guadalupe García Moncayo.
Redacción – revisión y edición: Glenda Marcela Sarmiento Tomalá, Zoraida Burbano Gómez, Pilar Asunción Soledispa Cañarte, Alexandra López Barrera, Francisca Patricia Jimenez Granizo, María Guadalupe García Moncayo.