doi: 10.56294/hl2023228
ORIGINAL
Pharmacological study and nutritional value of Amaranthus dubius Mart. leaves (Bledo)
Estudio farmacológico y valor nutricional de las hojas Amaranthus dubius Mart (Bledo)
Escobar Paredes Rebeca Lucrecia1, Solís Monar Lissette
Gabriela1, Pilar Asunción Soledispa Cañarte1
![]()
1Universidad de Guayaquil, Facultad de Ciencias Químicas. Guayaquil, Ecuador.
Citar como: Escobar Paredes RL, Solís Monar LG, Soledispa Cañarte PA. Pharmacological study and nutritional value of Amaranthus dubius Mart. leaves (Bledo). Health Leadership and Quality of Life. 2023; 2:228. https://doi.org/10.56294/hl2023228
Enviado: 25-04-2023 Revisado: 10-07-2023 Aceptado: 10-10-2023 Publicado: 11-10-2023
Editor:
PhD. Prof. Neela Satheesh ![]()
ABSTRACT
The objective of this research is to study the pharmacognostic characteristics and to know the nutritional value of the leaf of Amaranthus dubius Mart. obtained from the Durán canton of the province of Guayaquil. Part of the analyses were carried out in the “Food Laboratory of the Faculty of Chemical Sciences” of the University of Guayaquil and the other part in the “AGRORUM Laboratory”; obtaining as a result the pharmacognostic parameters: total ashes 20 %, water soluble ashes 5,25 %, insoluble ashes in hydrochloric acid 14,3 %, humidity 8 %, soluble substances 5,2 % (Ext. aqueous), 2,2 % (Ext. ethereal), 2,80 % (Ext. alcoholic), using the Miranda and Cuellar method. Phytochemical screening was used to qualitatively determine the presence of alkaloids, quinones, flavonoids, fatty acids, reducing sugars, phenolics and/or tannins and triterpenes and/or steroids, following the Miranda and Cuellar methodology. For the determination of the nutritional value, parameters such as macronutrients (phosphorus (0,13 %), magnesium (0,20 %), nitrogen (4,71 %), potassium (1,67 %), calcium (0,16 %) and sulfur (0,09 %)), micronutrients (Iron (149,07mg/kg), Zinc (88,71mg/kg), Copper (18,69mg/kg), Manganese (147,28mg/kg), Boron (17,80mg/kg) and Sodium (84,15 mg/kg)) and fiber (16,94) by internal laboratory technique.
Keywords: Amranthus dubius; Leaves; Nutritional; Phytochemical Screening; Pharmacognostic Characteristics; Pharmacognostic Characteristics.
RESUMEN
La presente investigación tiene como objetivo estudiar las características farmacognósticas y conocer el valor nutricional de la hoja de Amaranthus dubius Mart. obtenida del cantón Durán de la provincia de Guayaquil. Una parte de los análisis se realizaron en el “Laboratorio de Alimentos de la Facultad de Ciencias Químicas” de la Universidad de Guayaquil y la otra parte en el “Laboratorio de AGRORUM”; obteniendo como resultado los parámetros farmacognósticos: cenizas totales 20 %, cenizas solubles en agua 5,25 %, cenizas insolubles en ácido clorhídrico 14,3 %, humedad 8 %, sustancias solubles 5,2 % (Ext. Acuoso), 2,2 % (Ext. Etéreo), 2,80 % (Ext. alcohólico), utilizando el método de Miranda y Cuéllar. Mediante el tamizaje fitoquímico se determinó cualitativamente la presencia de alcaloides, quinonas, flavonoides, ácidos grasos, azúcares reductores, fenólicos y/o taninos y triterpenos y/o esteroides, siguiendo la metodología de Miranda y Cuéllar. Para la determinación del valor de nutricional se realizó parámetros como macronutrientes (fósforo (0,13 %), Magnesio (0,20 %), Nitrógeno (4,71 %), Potasio (1,67 %), Calcio (0,16 %) y Azufre (0,09 %), micronutrientes (Hierro (149,07mg/kg), Zinc (88,71mg/kg), Cobre (18,69mg/kg), Manganeso (147,28mg/kg), Boro (17,80mg/kg) y Sodio (84,15 mg/kg) y fibra (16,94) mediante técnica interna del laboratorio.
Palabras clave: Amranthus Dubius; Hojas; Nutricional; Tamizaje Fitoquímico; Características Farmacognósticos.
INTRODUCCIÓN
Dentro del género Amaranthus se estiman de 60 a 75 especies conocidas en todo el mundo, entre las cuales la mayoría de ellas provienen de América y solo 15 especies son de Europa, Asia, África y Australia, por lo cual muchas de sus características dependen del medio donde se desarrollan, dando así múltiples variaciones de especies.(1,2,3)
El género Amaranthus se caracteriza por su alto contenido de nutrientes tanto en hojas como en las semillas, además de sus diferentes propiedades medicinales, en este caso se centra en las hojas de la Amaranthus dubius Mart. o mayor conocida como bledo o pira.(4,5,6) Sus hojas tienen múltiples propiedades y beneficios que ayudan a combatir la diarrea, la menstruación, úlceras cutáneas, tos, fiebre, entre otras características además de esto es un gran oxigenante cerebral y un estimulante neuronal.(7,8,9)
Entre la composición de las hojas se encuentra diferentes componentes como calcio, potasio, fósforo, magnesio, hierro, zinc, cobre, vitamina B1 o tiamina, B2 o riboflavina, B3, A y C, aminoácidos, entre otros.(10,11,12)
Por lo tanto, se realiza la propuesta de identificar mediante tamizaje fitoquímicos los metabolitos y el valor nutricional presente en las hojas de Amaranthus dubius Mart. con la finalidad de conocer su potencial como posible alimento.
¿Qué características farmacognósticas y valor nutricional presentarán las hojas Amaranthus dubius Mart obtenido del cantón Durán?
Objetivo
Estudiar las características farmacognósticas y el valor nutricional de las hojas de Amaranthus dubius Mart. (Bledo)
MÉTODO
Tipo de investigación El presente trabajo de investigación es de tipo experimental y bibliográfico. Experimental dado que se llevó a cabo la evaluación de los extractos, donde la realización de los estudios farmacognósticos se desarrolló en el Laboratorio de alimentos de la Facultad de Ciencias Químicas de la Universidad de Guayaquil, y la determinación del valor nutricional por parte de los Laboratorios de Agrorum.
Bibliográfico ya que se consultó con información científica para ampliar los conocimientos de la especie y la metodología aplicada.
Estudio farmacognotico
Recolecccion, ,selección e identificación: Las hojas de la especie se recolectaron en el cantón Durán en el mes de noviembre del 2022.
Para la identificación de la especie “149” se llevó la planta completa al Herbario GUAY de la Facultad de Ciencias Naturales de la Universidad de Guayaquil.
Secado, molida y almacenamiento: una vez realizada la identificación, se procedió con la recolección de las hojas de la especie para luego clasificarlas y secarlas a temperatura ambiente. Después del tiempo trascurrido se pulverizó las hojas en un mortero, para luego pasarla por un tamiz y almacenarlas en un frasco de vidrio con tapa hermética y cubiertas con papel aluminio para su posterior análisis.
Macroformologia: la descripción macromorfología de las hojas de Amaranthus dubius se llevó a cabo mediante la observación y se evaluó los siguientes aspectos: tamaño, forma, color, condición y caracteres de la superficie
Parámetros fisicoquimicos
Determinación de cenizas totales: la Determinación de cenizas totales es una técnica que nos permite medir el total de materia que queda después de una calcinación, por lo cual esto incluye cenizas fisiológicas que son tejidos provenientes de la planta y las cenizas no fisiológicas que son materia extraña que se encuentra en la superficie de la especie.
|
Tabla 1. Materiales y equipos para la determinación de cenizas |
|
|
Crisoles |
Pinza |
|
Agua destilada |
Vasos de precipitación |
|
Papel filtro |
Pipetas |
|
Desecador |
Balanza digital marca SHIMADZU |
|
Calentador u hornilla de calentamiento |
Mufla marca MLW |
|
Estufa Marca MEMMERT |
Mechero |

Fuente: Miranda et al.
Figura 1. Procedimiento de Cenizas Totales
Expresión de los resultados:

Ct = Porcentaje de cenizas totales en base hidratada.
M = Masa del crisol vacío (g).
M1 = Masa del crisol con la porción de ensayo (g).
M2 = Masa del crisol con la ceniza (g).
100 = Factor matemático para los cálculos.
Determinación de cenizas solubles en agua

Fuente: Miranda et al.
Figura 2. Procedimiento de Cenizas solubles en agua
Gráfico: Expresión de resultados:
![]()
Ca = Porcentaje de cenizas solubles en agua en base hidratada.
M2 = Masa del crisol con las cenizas totales (g).
Ma = Masa del crisol con las cenizas insolubles en agua (g).
M1 = Masa del crisol con la muestra de ensayo (g).
M = Masa del crisol vacío (g).
100 = Factor matemático.
Determinación de cenizas insolubles en ácido clorhídrico

Figura 3. Procedimiento de Cenizas insolubles en ácido clorhídrico
Expresión de resultados:
![]()
Cac = Porcentaje de cenizas insolubles en ácido clorhídrico en base hidratada. M1 = Masa del crisol con la porción de ensayos (g).
M = Masa del crisol vacío (g).
M2 = Masa del crisol con la ceniza (g).
100 = Factor matemático.
Determinación de humedad
La determinación de humedad se lleva a cabo mediante el método gravimétrico donde en el cual denota la pérdida de masa después de un proceso de desecado en la estufa.
|
Tabla 2. Materiales y equipos para la determinación de humedad |
|
|
Capsulas |
Pinza |
|
Espátula |
Estufa Marca MEMMERT |
|
Desecador |
Balanza digital marca SHIMADZU |

Fuente: Miranda et al.
Figura 4. Procedimiento para la determinación humedad
Expresión de los resultados:
![]()
Hg = Pérdida en peso por desecación (%).
M2 = Masa de la cápsula con la muestra de ensayos (g).
M1 = Masa de la cápsula con la muestra de ensayo desecada (g).
100 = Factor matemático.
M = Masa de la cápsula vacía.
Determinación de sustancias solubles
En la determinación de sustancias solubles se utilizan solventes como éter, agua, alcohol entre otros, donde mediante una maceración se obtienen extractos de estas sustancias en donde se ocupará alícuotas de los extractos hasta su sequedad.

Figura 5. Procedimiento para la determinación de sustancias solubles
Estudio fitoquímico
Tamizaje fitoquímico
El tamizaje Fitoquímico nos ayuda a
tener conocimiento de que metabolitos se encuentran presentes en las hojas de
Amaranthus dubius Mart utilizando extracciones que se fueron obtenidas mediante
maceraciones en diferentes solventes. El tamizaje fitoquímico se basó en la
metodología propuesta por Miranda Martínez et al.
|
Tabla 3. Materiales y equipos para el Tamizaje Fitoquímico |
|
|
Sorbona |
Embudo |
|
Agua destilada |
Vasos de precipitación |
|
Papel filtro |
Pipetas |
|
Varilla de vidrio |
Frascos de vidrio |
|
Hornilla de calentamiento |
Gradilla |
|
Tubos de ensayo |
Cucharilla |
|
Tabla 4. Reactivos a ocupar para el tamizaje Fitoquímico |
|
|
Éter etílico |
Etanol |
|
Agua destilada |
Sudan III |
|
Fehling B |
Fehling A |
|
Cloruro férrico |
Cloroformo |
|
Ácido clorhídrico conc. y al 1 % |
Anhídrido acético |
|
Hidróxido de sodio 10 % y 5 % en agua |
Alcohol amílico |
|
Ácido pícrico 1 % en etanol |
Cinta de magnesio |
|
Acetato de sodio |
|
Preparación de la muestra

Fuente: Miranda et al.
Figura 6. Esquema de la preparación de la muestra para la obtención de los extractos
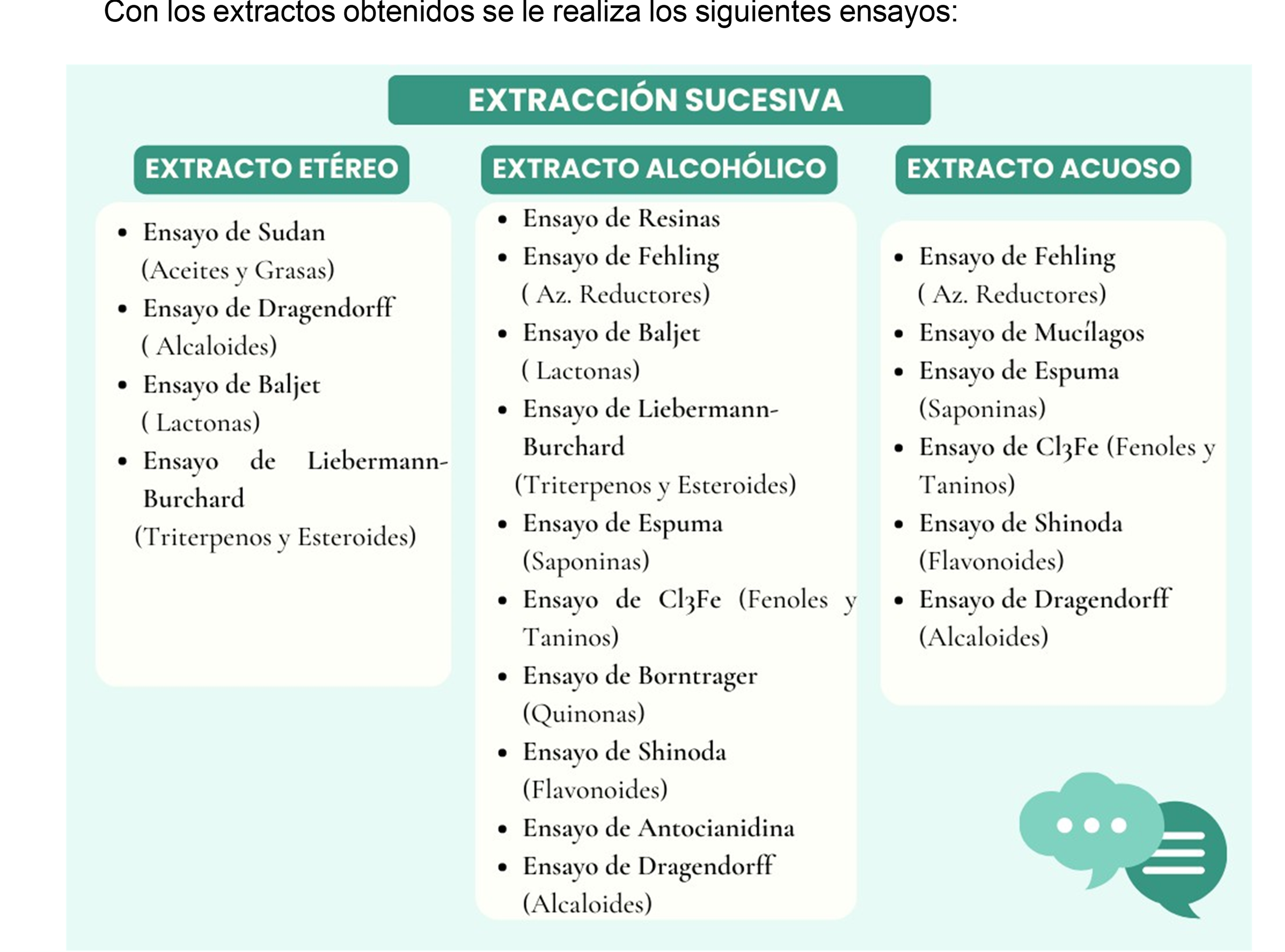
Fuente: Miranda et al.
Figura 7. Ensayos realizados con el extracto etéreo, alcohólico y acuoso
Ensayo de Sudan: permite reconocer la presencia de compuestos grasos. En un tubo de ensayo se coloca 1 ml del extracto y se le adiciona 1 ml del reactivo Sudan III o Sudan IV, se calienta en baño de agua hasta la evaporación del solvente. El resultado es positivo si aparecen gotas o una película coloreada de rojo en las paredes del tubo de ensayo.
Ensayo de Baljet: permite reconocer la presencia de compuestos con agrupamiento lactónicos, en particular coumarinas u otros compuestos lactónicos. En un tubo de ensayo se agrega 1 ml del extracto; si el extracto no es alcohólico, se debe evaporar en baño María y redisolverse en 1 ml de etanol. Luego se adiciona 1 ml del reactivo Baljet, considerándose un ensayo positivo la aparición de coloración (++) o precipitado rojo (+++).
El reactivo Baljet se prepara con Hidróxido de sodio al 10 % en agua y Ácido pícrico al 1 % en etanol, ambas soluciones se preparan de forma independiente y se mezcla en igual cantidad al momento de realizar el ensayo.
Ensayo de Dragendorff: permite reconocer la presencia de alcaloides. Si el extracto se encuentra disuelto en un solvente orgánico, se debe evaporar en baño María y el residuo redisolverse en 1 ml de ácido clorhídrico al 1 % en agua. Si el extracto es acuoso, se le agrega 1 gota de ácido clorhídrico concentrado, (calentar suavemente y dejar enfriar hasta acidez). Con la solución acuosa ácida se realiza el ensayo, añadiendo 3 gotas del reactivo de Dragendorff, si hay opalescencia se considera positiva (+), turbidez definida (++), precipitado (+++).
Ensayo de Liebermann-Burchard: permite reconocer la presencia de triterpenos y esteroides. En un tubo de ensayo se agrega 1 ml del extracto si el extracto no se encuentra en cloroformo, se debe evaporar en baño María y el residuo redisolverse en 1 ml de cloroformo. Se agrega 1 ml de anhídrido acético y se mezcla homogéneamente. Se adiciona por las paredes del tubo de 2 a 3 gotas de ácido sulfúrico concentrado sin agitar. Un ensayo positivo se puede reconocer por cambios rápido de coloraciones:
1. Rosado-azul (Muy rápido).
2. Verde intenso (Visible, aunque rápido).
3. Verde oscuro-negro (Final de la reacción).
El ensayo puede quedar en dos fases o desarrollo de color. Muy pocas veces puede observarse el primer cambio. El tercer cambio suele ocurrir cuando el material evaluado tiene cantidades importantes de estos compuestos.
Ensayo de resinas: para detectar este tipo de compuesto, en un tubo de ensayo se agrega 1 ml del extracto alcohólico y 5 ml de agua destilada. El ensayo es positivo si aparece un precipitado.
Ensayo de Fehling: permite reconocer la presencia de azúcares reductores. En un tubo de ensayo se agrega 1 ml del extracto; si el extracto no es acuoso, se debe evaporar en baño María y el residuo redisolverse en 1-2 ml de agua. Se adiciona1 ml del reactivo y se calienta en baño de agua 5-10 minutos la mezcla.
El ensayo se considera positivo si la solución se colorea de rojo o aparece precipitado rojo.
Ensayo de la espuma: permite reconocer la presencia de saponinas, tanto del tipo esteroidal como triterpénica. En tubo de ensayo se agrega 1 ml del extracto alcohólico y se diluye con 5 veces su volumen en agua y se agita la mezcla fuertemente durante 5-10 minutos. El ensayo es positivo si aparece espuma en la superficie del líquido de más de 2 mm de altura y persistente por más de 2 minutos.
Ensayo de Cloruro Férrico: permite reconocer la presencia de compuestos fenólicos y taninos. En extracto alcohólico, determina tanto fenoles como taninos y en acuoso determina taninos. En un tubo de ensayo se coloca 1 ml del extracto; si el extracto es alcohólico se agrega 3 gotas de una solución de tricloruro férrico al 5 % en solución salina fisiológica. Si el extracto es acuoso, se le añade acetato de sodio para neutralizar y 3 gotas de una solución de tricloruro férrico al 5 % en solución salina fisiológica. Un ensayo positivo puede dar la siguiente información general:
· Desarrollo de una solución rojo-vino: compuestos fenólicos en general
· Desarrollo de una solución verde intensa: taninos del tipo pirocatecólicos.
· Desarrollo de una coloración azul, taninos del tipo pirogalotánicos.
Ensayo de Borntrager: este ensayo permite identificar quinonas. Para ello si la alícuota del extracto no se encuentra en cloroformo, debe evaporarse el solvente en baño maría y el residuo redisolverse en 1 ml de cloroformo. Se adiciona 1 ml de hidróxido de sodio. Se agita mezclando las fases y se deja en reposo hasta su separación. Si la fase acuosa alcalina (superior) se colorea rosado o rojo se considera positivo. Coloración rosada (++), coloración roja (+++).
Ensayo de Shinoda: permite reconocer la presencia de flavonoides. En un tubo de ensayo se coloca 1 ml del extracto, si el extracto se encuentra en alcohol, se diluye con 1 ml de ácido clorhídrico concentrado y un pedacito de cinta de magnesio metálico. Después de la reacción se espera 5 minutos, se añade 1 ml de alcohol amílico, se mezclan las fases y se deja reposar hasta que se separen. Si el extracto es acuoso se procede de igual forma, a partir de la adición del ácido clorhídrico concentrado. El ensayo se considera positivo, cuando el alcohol amílico se colorea de amarillo, naranja, carmelita o rojo; intensos en todos los casos.
Ensayo de Antocianidinas: permite reconocer la presencia de estructuras de secuencia C6-C3-C6 del grupo de los flavonoides. En un tubo de ensayo colocar 1 ml del extracto etanólico con 0,5 ml de HCL conc., se calienta por 10 minutos, se deja enfriar y se adiciona 1 ml de agua y 2 ml de alcohol amílico.
Se agita y se deja separar las dos fases. La aparición de color rojo a marrón en la fase amílica, es indicativa de un ensayo positivo.
Ensayo de mucílagos: permite reconocer en los extractos de vegetales la presencia de esta estructura tipo polisacárido, que forma un coloide hidrófilo de alto índice de masa que aumenta la densidad del agua donde se extrae. En un tubo de ensayo se coloca 1 ml del extracto acuoso y se enfría a 0 – 5 ºC y si la solución toma una consistencia gelatinosa el ensayo es positivo.
Valor nutricional
El valor nutritivo de una planta está dado por su composición química por lo cual es muy importante conocer el contenido de nutrientes presentes. Por esta razón para conocer su valor nutricional se realizó un examen foliar básico que comprende proteínas, minerales y fibra basándose en la metodología de los métodos de la Association of Official Analitycal Chemists y metodología aplicada por los laboratorios de AGRORUM.
Análisis foliar básico
Determinación de nitrógeno total (NT)
Para la determinación de Nitrógeno Total (NT) se emplea el método Kjeldahl, donde la muestra es descompuesta en caliente en un medio ácido (ácido sulfúrico), en presencia de un agente reductor catalizador (mercurio, cobre o selenio). Luego se adiciona una sal neutra para aumentar el punto de ebullición (337 °C) de la disolución de ácido sulfúrico. De esta forma que aumenta temperatura de trabajo, con lo cual se favorece la descomposición logrando la destilación en corriente de vapor.
El frasco colector contiene un volumen medido de una disolución estándar de ácido, al finalizar la destilación se procede a valorar el ácido no consumido con una disolución de base patrón. El volumen de disolución básica consumido hasta llegar al punto de equivalencia permite conocer la cantidad de NH3, y de esta forma, la cantidad de nitrógeno en la muestra.
Determinación fósforo (P) por espectrofotometría UV- VIS
Se purga todo el material a utilizar con HCL, de tal manera se evita cualquier tipo de interferencia en la corrida de la muestra. Se prepara la muestra patrón a 50 ppm de concentración y almacena en un frasco ámbar, en donde a partir de la solución patrón preparada anteriormente se diluye a 100 ml de 10 ppm en balón volumétrico. Con la solución patrón de 10 ppm se realiza las siguientes concentraciones: 0,01, 0,05, 0,1, 0,3, 0,5, 1,0 mg del ion fosfato en los respectivos balones volumétricos 100 ml, y un duplicado de concentración 0,3, de la misma manera se elabora un blanco de 100 ml. Finalmente se agrega la muestra a un balón volumétrico 100 ml con 4 ml de molibdato de amonio a cada balón para formar fosfomolibdato de amonio. En el caso del duplicado de concentración 0,3 se adicionó 10 gotas de cloruro estañoso con glicerol, dejando reposar 11 minutos. Pasados los 11 minutos se toma la longitud de onda al duplicado en el espectrofotómetro. Con la longitud de onda obtenida se calibra el equipo con el que se va a trabajar para medir los grados de absorbancia obteniendo la curva de calibración. La primera medición que se realiza fue solo agua destilada en la celda, posteriormente se agrega 10 gotas el cloruro estañoso desde el blanco hasta la muestra por intervalos de 2 minutos. Iniciando la medición de la absorbancia pasado 10 minutos de haber agregado el cloruro estañoso. Para la medición de la absorbancia se agrega a la celda del espectrofotómetro una pequeña muestra de cada balón, realizando un lavado previo con agua destilada.
Determinación de sodio (Na), potasio (K), calcio (Ca), magnesio (Mg), Hierro (Fe), zinc (Zn), cobre (Cu), manganeso (Mn), boro (B)
Para el tratamiento de la muestra se debe pesar 1 g de la planta seca y molida, luego de esto se debe colocar en un tubo de plastico agregando 10mL de ácido nitrico concentrado (HNO3), donde el frasco reposa durante 12h, a la par de la muestra se debe preparar el blanco con la muestra de referencia. Pasado el tiempo de posa se debera calentar en el bloque de digestion de Evironmental Express a 105oC , se le debe colocar la tapa de salida de vapores hasta la produccion de humos rojos de NO2 haya cesado(en caso de que falte de digestar la muestra, se anade 2mL de HNO3 concentrado para que continue su proceso de digestion). Al finalizar se debe dejar enfriar el tubo con la digestion a temperatura ambiente y agregar una pequena cantidad de Ácido perclórico HClO4 AL 70 %. Se debe calentar nuevamente a la temperatura de 105oC dejando que se evapore hasta obtener un volumen pequeño (menor o igual a 5ml).
Se deja enfriar y se transfiere la muestra digestada a un matraz de volumen 50mL, haciendo enjuages de la tapa y frasco con agua ultrapura seguidamente con la aforacion con agua tipo reactivo. Se debe filtrar con papel filtro cuantitativo, ese filtrado se lo puede utilizar para las lecturas en el espectrofotometro de absorcion atomica. Se debe encender el espectrofotometro de absorcion atomica, dejando calentar la lampara a utilizar por lo menos 30min. El EAA con llama de aire-acetileno C2H2 y calibrado con la serie de estandares (Ca= 422,67; Mg=285,21 ; K=766,49; Na=589; Cu=324,75; Fe=248,33; Mn=279,48 y Zn=213,86).
La parte instrumental se acondiciona el EAA siguiendo los pasos del manual de uso, se prosigue con la lectura de los estandares, blanco y lote de muestras a analizar. Donde el coeficiente de correlacion para cada analito debe ser ≥0,99. El RSD de las intensida de absorbancia: la dispersion de los valores experimentales de la curva respecto al valor teorico no debe ser mayor a 15 %. Para el cálculo de la concentracion en mg/L se emplea la siguiente formula:
Conc.(mg/L)=Abs ±b/a*Fd
Donde:
Abs: absorbancia de la muestra
b: pendiente de la curva
a: intercepto
Fd: Fator de dilución
Determinación de fibra cruda
Se realiza la digestión con soluciones de ácido sulfúrico e hidróxido de sodio, posteriormente se calcina el residuo. Se pesa 1 g de muestra desengrasada y se le adiciona 100 ml de ácido sulfúrico al 1,25 %. Se calienta en la plancha de calentamiento, por 30min. Seguidamente se filtra por un papel de filtro previa- mente tarado y se le adiciona 100ml de NaOH al 1,25 % (p/v) y se coloca nuevamente en la plancha de calentamiento por 30min. Posteriormente se filtra y se lava con etanol absoluto; el papel de filtro con el residuo se lleva a secar a la estufa por 24h. Se pasa el papel a un crisol previamente tarado y se pesa para posteriormente quemar y poner en la mufla por 8h; pasado este tiempo se sacó de la mufla, se enfrió y se pesó. El porciento de fibra se determinó según la siguiente ecuación:
![]()
Donde:
W1= Peso de la muestra.
W3= peso de crisol más muestra seca.
W4= peso de crisol + ceniza.
RESULTADOS Y DISCUSIÓN
A continuación, se muestra la descripción macromorfológica de las hojas de Amaranthus dubius:

Figura 8. Macromorfología de las hojas
Parámetros fisicoquímicos
En las siguientes figuras se reflejan los resultados de los ensayos fisicoquímicos realizados a la hoja pulverizada de la planta de Amaranthus dubius.(13,14,15,16) Dichos resultados fueron comparados con los valores de diferentes estudios realizados en la hoja del bledo, cabe mencionar también que hay resultados que no existen estudios realizados y se presentan por primera vez.(17,18)
Cenizas totales
El ensayo de cenizas totales es un parámetro de calidad para indicar el porcentaje de minerales que se encuentran presente en la muestra.(19,20) Este ensayo se realizó por duplicado y se obtuvo como resultado 20 %, comparando estos resultados con los obtenidos en el trabajo desarrollado por un estudio de la composición química del Amaranthus dubius donde indicaron el valor de 20,18 % para cenizas, se puede indicar que los porcentajes son cercanos.(21,22,23) Sin embargo, de acuerdo a la Farmacopea china establece un porcentaje referencial al 15 % de cenizas totales para materia vegetal.(24,25,26)

Figura 9. Porcentaje de cenizas totales
Cenizas solubles en agua
El análisis de cenizas solubles en agua, es el contenido de cenizas totales disueltas en agua, en la determinación de este ensayo se realizó por duplicado dando como resultado un promedio de 5,25 % con una desviación estándar de 0,75. Para este parámetro no existe antecedentes por lo cual se registra como primera vez.(27,28,29)
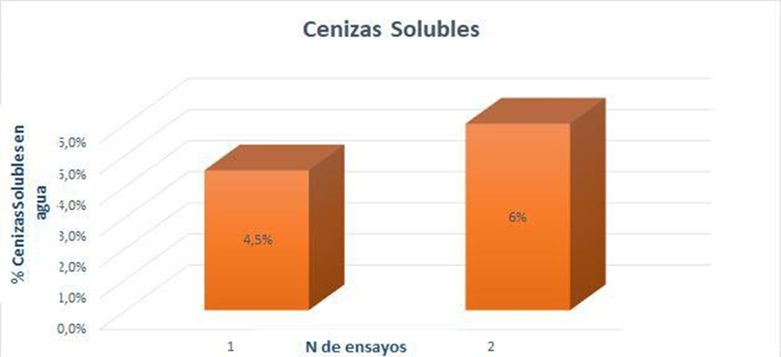
Figura 10. Porcentaje de cenizas solubles en agua
Cenizas insolubles en ácido clorhídrico
En el análisis de cenizas insolubles en ácido clorhídrico se determina la cantidad de sílice, este ensayo se realizó por duplicado dando un porcentaje de 14,3 %.(30,31,32) Estos resultados se presentan por primera vez.
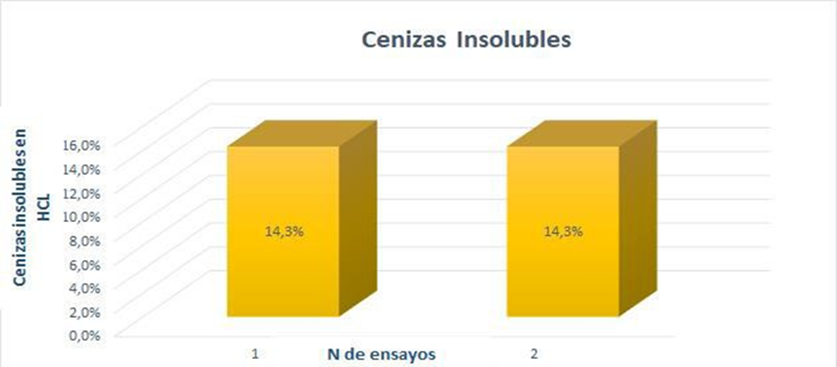
Figura 11. Porcentaje de cenizas insolubles en HCl
Humedad
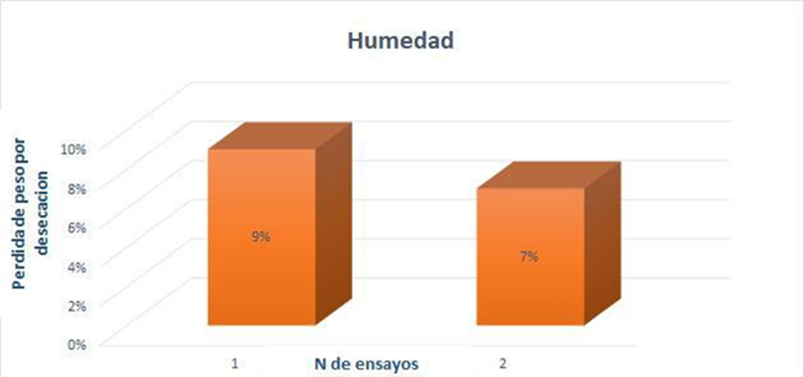
Figura 12. Porcentaje de humedad
En este ensayo se determinó la pérdida de peso por desecación, este análisis se realizó por duplicado dando como promedio 8 % y una desviación estándar de 1.(33,34,35) No existe antecedentes de este parámetro, por ende, el resultado se presenta por primera vez.
Sustancias solubles
En la figura 13 se muestran los resultados obtenidos de las sustancias solubles realizadas en extracto acuoso, etéreo y alcohólico de las hojas de Amaranthus dubius, donde se obtuvo un porcentaje de etéreo de 2,2 % comparándolo con la investigación de un estudio donde sus resultados reflejan que tiene un porcentaje de 1,28 ± 0,85 lo cual indica porcentajes cercanos mientras que el extracto acuoso y el alcohólico no existen antecedentes, por lo tanto, el resultado se presenta por primera vez.(36,37,38)
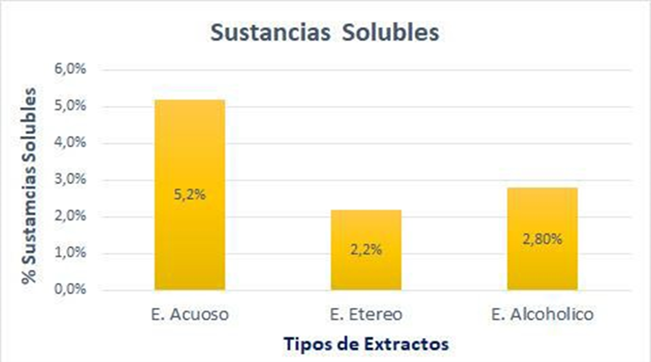
Figura 13. Porcentaje de las sustancias solubles
Tamizaje fitoquímico
En la tabla 5 se presentan los resultados del tamizaje de fitoquímico realizado con los extractos etéreo, acuoso y alcohólico de las hojas pulverizadas de la planta de Amaranthus dubius.
|
Tabla 5. Resultados del tamizaje fitoquímico |
||||
|
Metabolitos |
Extractos |
|||
|
Etéreo |
Alcohólico |
Acuoso |
||
|
Sudan |
Compuestos grasos |
+ |
N/A |
N/A |
|
Baljet |
Cumarinas |
- |
- |
N/A |
|
Dragendorff |
Alcaloides |
- |
+++ |
+ |
|
Liberman- Burchard |
Triterpenos y/o Esteroides |
+ Verde esmeralda |
- |
N/A |
|
Resinas |
Resina |
N/A |
- |
N/A |
|
Fehling |
Azucares Reductores |
N/A |
+++ |
+++ |
|
Espuma |
Saponinas |
N/A |
- |
N/A |
|
Cloruro Férrico |
Fenólicos y/o Taninos |
N/A |
+ Verde oscuro |
+ Azul oscuro |
|
Borntrager |
Quinonas |
N/A |
++ |
N/A |
|
Shinoda |
Flavonoides |
N/A |
+ Amarillo |
+ Amarillo naranja |
|
Antocianidinas |
Antocianidina |
N/A |
- |
N/A |
|
Mucílagos |
Estructuras Tipo Polisacáridos |
N/A |
N/A |
- |
Mediante el estudio Fitoquímico realizado a la hoja de Amaranthus dubius empleando la metodología de un estudio se denotó que en el extracto etéreo se encuentran compuestos grasos y triterpenos y/o esteroides más en el extracto alcohólico y acuoso se hallaron presentes metabolitos como alcaloides, azúcares reductores, fenólicos y/o taninos, flavonoides y quinonas, este último se identificó solamente en el extracto alcohólico.(39,40)
Por otro lado, en la determinación foliar de Amaranthus caudatus que realiza Jessica Guapi en su tesis, se encontró similitudes en cuanto a los resultados de las especies a considerar, más se destaca el hecho de que no se halló presente alcaloides y quinonas en la tesis de referencia, sin embargo, en las hojas de Amaranthus dubius se presentó en el extracto acuoso una opalescencia (+) y precipitación en el extracto alcohólico mientras que en la identificación de quinonas se observó una coloración rosada (++) confirmando la presencia de una quinona.(41,42,43)
Valor nutricional
El contenido de macronutrientes, micronutrientes y fibra seca se desarrolló empleando un análisis foliar, proporcionando los resultados detallados a continuación:
|
Tabla 6. Resultados del examen foliar básico |
|
|
Contenido de nutrientes en hojas de Amaranthus dubius Mart |
|
|
Macronutrientes |
Concentración por cada gramo de muestra (% s.m.s) |
|
Nitrógeno (N) |
4,71 % |
|
Fósforo (P) |
0,13 % |
|
Magnesio (Mg) |
0,20 % |
|
Potasio (K) |
1,67 % |
|
Calcio (Ca) |
0,16 % |
|
Azufre (S) |
0,09 % |
|
Micronutrientes |
Concentración por cada gramo de muestra (mg/kg) |
|
Hierro (Fe) |
149,07 mg/kg |
|
Zinc (Zn) |
88,71 mg/kg |
|
Cobre (Cu) |
18,69 mg/kg |
|
Manganeso (Mn) |
147,28 mg/kg |
|
Boro (B) |
17,80 mg/kg |
|
Sodio (Na) |
84,15 mg/kg |
|
Fibra |
Concentración por cada gramo de muestra(%p/p) |
|
Fibra cruda |
16,94 % |
La determinación de los diferentes analices descriptos en la tabla 6 dieron como resultado las siguientes aportaciones:
Macronutrientes: el contenido de nitrógeno fue estimado en 4,71 %, un valor esperado dado las características nutricionales de la planta, el porcentaje obtenido cumple el rango óptimo proporcionado por parte del laboratorio, además se realizó la comparación con los rangos descriptos en el manual de agronomía(44,45) para el caso de la lechuga y la espinaca, evidenciando que cumple el contenido nutricional para usos alimenticios.(46,47)
El contenido de fósforo, Magnesio, Potasio, Calcio y Azufre resultan con un valor inferior al esperado, pues no se encuentra dentro del rango de referencia otorgado por el laboratorio, más, sin embargo, se puede inferir que los factores externos a la planta hubiesen interferido en el contenido de estos macronutrientes.(48,49)
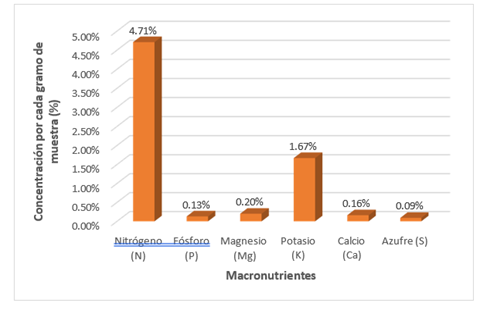
Figura 14. Porcentaje de macronutrientes
Micronutrientes: en el caso del Hierro, Zinc, Cobre, Manganeso, Boro y Sodio se puede destacar que la hoja se encuentra enriquecida con la presencia de estos micronutrientes, pues cumple con sobremanera los rangos aceptados para la lechuga y espinaca.(50,51)

Figura 15. Resultados de los micronutrientes
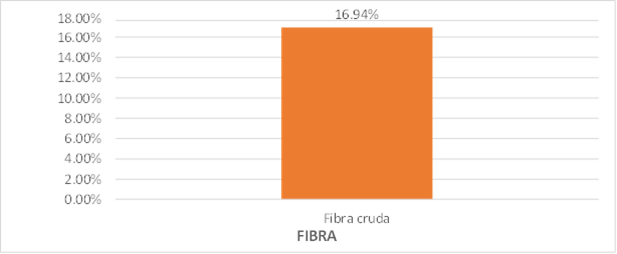
Figura 16. Porcentaje de Fibra cruda
Fibra: en el contenido de fibra cruda fue estimado en 16,94 %, en este caso no se proporcionó un rango de referencia por parte del laboratorio, pero, sin embargo, se realiza la comparación con el artículo de referencia,(52,53) el mismo que indica un valor de 9,24 % se puede inferir que los factores externos a la planta hubiesen interferido en el contenido de fibra.(54,55)
CONCLUSIONES
El herbario GUAY identificó con el número “149” la muestra vegetal y la clasificó como Amaranthus dubius Mart.
Se estableció mediante parámetros fisicoquímicos las propiedades de las hojas de Amaranthus dubius Mart. se estimaron: cenizas totales, cenizas insolubles en agua, cenizas insolubles en ácido clorhídrico, humedad, sustancias solubles en extracto acuoso, extracto etéreo, extracto alcohólico.
Se determinó mediante el tamizaje fitoquímico la composición química cualitativa en los extractos etéreo, alcohólico y acuoso de las hojas de Amaranthus dubius Mart. encontrando la presencia de metabolitos tales como: alcaloides, quinonas, flavonoides, compuestos grasos, Triterpenos y/o esteroides, azúcares reductores, fenólicos y/o taninos.
Se definió el valor nutricional de micronutrientes y proteínas contenido en las hojas de Amaranthus dubius Mart., evidenciando que las hojas de tienen potencial dentro del uso de la alimentación.
REFERENCIAS BIBLIOGRÁFICAS
1. Peralta E, Mazón N, Murillo Á, Minchala L. Evaluación del amaranto en la provincia de Santa Elena, Ecuador. 2016.
2. Sánchez Y. Un alimento ancestral subvalorado que crece por donde caminas [Internet]. Juventud Rebelde. 2018 [cited 2022 Mar 5]. Available from: https://www.juventudrebelde.cu/ciencia-tecnica/2018-10-16/un-alimento-ancestral-subvalorado-que-crece-por-donde-caminas
3. Santos Rivera AL, Leones Cedeño AF, Chávez Arizala JF, Morales-García WC. Knowledge and practices on anemia in representatives of children under 5 years of age from the “Luz y Libertad” Educational Unit in La Concordia, 2023. Interamerican Journal of Health Sciences . 2023;3:170.
4. Olivares E, Peña E. Bioconcentración de elementos minerales en Amaranthus dubius (bledo, pira), creciendo silvestre en cultivos del estado Miranda, Venezuela y utilizado en la alimentación. Interciencia. 2009;34(9):604-11.
5. Montero K, Moreno R, Molina E, Sánchez AB. Composición química del Amaranthus dubius: una alternativa para la alimentación humana y animal. Rev Fac Agron [Internet]. 2011;28(1):619-27. Available from: https://www.revfacagronluz.org.ve/PDF/suplemento_diciembre_2011/v28supl1a2011ta_619.pdf
6. Gómez N. El súper alimento oxigenante cerebral que pasa desapercibido para muchos [Internet]. Aportes Nutricionales. 2018 [cited 2022 Mar 5]. Available from: https://actualidad.rt.com/actualidad/291787-super-alimento-oxigenante-cerebral-pasa-desapercibido
7. Guapi J. Caracterización bromatológica y fitoquímica de los granos y hojas del choco (Lupinus mutabilis Sweet), quinua (Chenopodium quinoa Willd), amaranto (Amaranthus caudatus L.) y sangorache (Amaranthus hybridus L.) [thesis]. Riobamba: Universidad Nacional del Chimborazo; 2014.
8. Dias A. Caracterización física, química, funcional y sensorial de hojas de amaranto (Amaranthus spp.) para consumo hortícola [thesis]. Santiago: Universidad de Chile; 2020.
9. Topón Jiménez ML, Lizcano-Ramirez JA, Morales-García WC. Educational interventions to combat anemia in pregnant women: nursing perspective. Interamerican Journal of Health Sciences. 2023;3:153.
10. Acevedo I, Garcia O, Acevedo I, Perdomo C. Valor nutritivo del bledo (Amaranthus spp) identificado en el Municipio Morán, Estado Lara. Rev Agrollanía. 2007;4:77-93.
11. Intriago C, Pérez P. Estudio del bledo (Amaranthus dubius) y sus aplicaciones culinarias en la gastronomía [thesis]. Guayaquil: Universidad de Guayaquil; 2017.
12. Molina P, Gonzalez P, Moreno R, Montero K, Ferrer R, Sanchez A. Sustancias tóxicas y antinutricionales de Amaranthus dubius Mart. ex Thell. Efecto de la parte de la planta y la época de recolecta. Rev Agron Univ Zulia. 2016;33:19-38.
13. Alonso J. Tratado de fitofármacos y nutracéuticos. In: Rosario - Argentina: Corpus Editorial; 2007. p. 46-8.
14. Nieto C. El cultivo de amaranto (Amaranthus spp.): una alternativa agronómica para Ecuador. 1989.
15. Walshaw S. Plant resources of tropical Africa. Bioone Complete. 2005 Aug;59(4):1-10.
16. Escobedo D. Generalidades de la Red Amaranto [Internet]. Servicio Nacional de Inspección y Certificación de Semillas. 2017 [cited 2022 Mar 5]. Available from: https://www.gob.mx/snics/acciones-y-programas/amaranto-amaranthus-spp
17. Luis G, Hernández B, Peña V, Torres N, Espinoza V, Ramírez L. Usos actuales y potenciales del amaranto (Amaranthus spp.). J Neg [Internet]. 2018 [cited 2022 Mar 5]. Available from: http://dx.doi.org/10.19230/jonnpr.2410
18. Ocampo JA, Barba de la Rosa AP. Caracterización bioquímica y estructural de las proteínas de reserva de amaranto. In: Espitia-Rangel E, editor. Amaranto: ciencia y tecnología. México: INIFAP/SINAREFI; 2012. p. 293-302.
19. Lipovestky F, Radrizani D, Guantay E E, Casabella C, Lattanzio B, Casanova M, et al. Enteral bile reinfusion in severe abdominal trauma. Interamerican Journal of Health Sciences. 2023;3:15
20. Elorza MS, Sánchez D, Sobrino E. Atlas de las plantas alóctonas invasoras en España. Organismo Autónomo Parques Nacionales; 2004.
21. Costea M, Tardif FJ. La biología de las malas hierbas canadienses. Amaranthus albus L., A. blitoides S. Watson y A. blitum L. Dep Agric Veg. 2003;30:1-10.
22. Carrera J. Los Amarantos [Internet]. ALLPA La voz de la tierra. 2020 [cited 2022 Mar 5]. Available from: https://www.allpa.org/los-amarantos
23. Aldas J, Jiménez E. Caracterización morfológica, física y fenológica de cuatro variedades de amaranto (Amaranthus sp.) para las condiciones meteorológicas del cantón Cevallos [thesis]. Cevallos: Universidad Técnica de Ambato; 2017.
24. Mosyakin SL, Robertson KR. Entrada para Amaranthus blitum Linnaeus [Internet]. Amaranto. 2001 [cited 2022 Mar 5]. Available from: https://plants.jstor.org/compilation/amaranthus.lividus
25. Merino O. Amaranthus lividus L [Internet]. Flora Vascular de Andalucía Occidental. 2017 [cited 2022 Mar 5]. Available from: https://www.floravascular.com/index.php?spp=Amaranthus%20lividus
26. Burgos R, Del Castillo A. Utilización de kiwicha precocida (Amaranthus caudatus) para el desarrollo de barras funcionales. Rev Chil Nutr. 2021;48(3).
27. Martínez L, Millán G, Rodríguez A, Montserrat M. Valor nutracéutico de la kiwicha (Amaranthus caudatus L.). Elsevier. 2020;65:13.
28. Martínez L, Millán G, Rodríguez A, Montserrat M. Valor nutracéutico de la kiwicha (Amaranthus caudatus L.). Elsevier. 2020 Feb;65:1-10.
29. Stüber K. Amaranthus caudatus Kiwicha [Internet]. 2004 [cited 2022 Mar 5]. Available from: caliban.mpiz-koeln.mpg.de/mavica/index.html
30. Acosta Sero O, Rey MS, Spehrs E. Factors associated with weight loss trajectory in adults after sleeve gastrectomy. Interamerican Journal of Health Sciences. 2023;3:144
31. Rangel E, Mapes E, Núñez C, Escobedo D. Recopilación y análisis de la información existente de las especies del género Amaranthus cultivadas y de sus posibles parientes silvestres en México. Rev Mex Cienc Agríc. 2010;1(3):427-37.
32. Livel K. Planta con flores Amaranthus hypochondriacus del Jardín Botánico de la Universidad Charles [Internet]. 2011 [cited 2022 Mar 5]. Available from: https://es.wikipedia.org/wiki/Amaranthus_hypochondriacus#/media/Archivo:Amaranthus_hypochondriacus_Prague_2011_1.jpg
33. Salazar F, Jaime M. Tamizaje fitoquímico en las hojas frescas de laurelillo [thesis]. Managua: Universidad Nacional Autónoma de Nicaragua; 2011.
34. Osorio C, Anthony C, Gamboa M, Susan C. Identificación de metabolitos secundarios presentes en la planta nativa cucharilla (Oreocallis grandiflora). Universidad Nacional del Callao; 2013.
35. Rodas B, Bressani R. Contenido de aceite, ácidos grasos y escualeno en variedades crudas y procesadas de grano de amaranto. 2009;59(1):1-10.
36. Potter NN, Hotchkiss JH. Ciencia de los alimentos. 15th ed. Zaragoza: Acribia; 1995.
37. Peñarrieta J, Tejada L, Mollinedo P, Vila J, Bravo J. Compuestos fenólicos y su presencia en alimentos. Rev Boliv Quím. 2014;31(2):1-6.
38. Ruiz A. Aminoácidos esenciales, cómo obtenerlos [Internet]. Consultas Nutricionales. 2017 [cited 2022 Mar 5]. Available from: https://www.webconsultas.com/dieta-y-nutricion/nutrientes/funciones-de-aminoacidos-esenciales
39. García Y, Meriño L, Morales N, Cassiani M, Alcalad L. Efecto de la inclusión de hojas de amaranto (Amaranthus dubius) en las propiedades de un yogur frutado. 2021;17(1). Available from: https://revistascientificas.cuc.edu.co/ingecuc/article/view/3221/3652
40. Díaz R. La pira: alimento de los dioses. Sevilla; 2011.
41. Carbajal Á. Manual de nutrición y dietética [Internet]. 2013 [cited 2022 Mar 5]. Available from: https://www.ucm.es/data/cont/docs/458-2013-07-24-cap-11-vitaminas.pdf
42. Speijers G. Glucósidos cianogenéticos [Internet]. Instituto Nacional de Salud Pública y Protección Ambiental. 2013 [cited 2022 Mar 5]. Available from: https://inchem.org/documents/jecfa/jecmono/v30je18.htm
43. Lluís J. Toxicología alimentaria. Natura Medicatrix. 2000;25(44):1-5.
44. Martínez L, Ibáñez R, Rincón E. Ácido fítico: aspectos nutricionales e implicaciones analíticas. Arch Latinoam Nutr. 2002;52(3):1-10.
45. Riverón B. Sustancias antinutricionales presentes frecuentemente en algunos alimentos [Internet]. Sustancias Nutricionales. 2021 [cited 2022 Mar 5]. Available from: https://actualfruveg.com/2021/08/22/sustancias-antinutricionales-alimentos/
46. Valdés A, Martí L, Salcedo C. Determinación de nitratos en vegetales. Rev Fac Cienc Agrar. 2004;23(1):1-6.
47. Chumpitaz-Saravia VL, Villaverde-Saravia B, Vivanco-Hilario SD, Morales-García WC. Nursing care in a postoperative adnexal cystectomypatient in the Obstetrics and Gynecology Service of anational hospital in Chincha, 2023. Interamerican Journal of Health Sciences. 2023;4:169
48. Iñigo S. Contaminantes: nitratos en productos vegetales y alimentos infantiles. 1st ed. McGraw Hill; 2011.
49. Orellana A. Catálogo de hortalizas nativas de Guatemala [Internet]. 2012 [cited 2022 Mar 5]. Available from:https://www.icta.gob.gt/publicaciones/Hortalizas%20nativas/Catalogo%20de%20hortalizas%20nativas%20de%20Guatemala,%202012.pdf
50. Algara P, Gallegos S, Reyes L. El amaranto y sus efectos terapéuticos. Rev Acad Investig. 2016;21:1-6.
51. Arabelovic S. Inhibidores del TNF [Internet]. Colegio Americano de Reumatología. 2022 [cited 2022 Mar 5]. Available from: https://www.rheumatology.org/I-Am-A/Patient-Caregiver/Tratamientos/Inhibidores-del-TNF
52. Miranda M, Cuéllar F. Farmacognosia y productos naturales. 2nd ed. Varela EF, editor. Cuba; 2012.
53. AOAC. Official methods of analysis. 15th ed. Washington, D.C.: Association of Official Analytical Chemists; 1990.
54. Cuello M, Jaramillo G, Canchingre F, Pérez JC, Castro C, Carrera O. Determinación de componentes nutricionales presentes en las hojas secas de Annona muricata L. (Guanábana). Rev Cumbres. 2017;3(1):1-6.
55. Laboratorio de México LA-L. Análisis foliares [Internet]. 2011 [cited 2022 Mar 5]. Available from: https://fuentesdeinformacioniapb.files.wordpress.com/2013/11/analisis-foliar.pdf
FINANCIACIÓN
Ninguna.
CONFLICTO DE INTERÉS
Los autores declaran que no existe conflicto de intereses.
CONTRIBUCIÓN DE AUTORÍA
Conceptualización: Escobar Paredes Rebeca Lucrecia, Solís Monar Lissette Gabriela, Pilar Asunción Soledispa Cañarte.
Curación de datos: Escobar Paredes Rebeca Lucrecia, Solís Monar Lissette Gabriela, Pilar Asunción Soledispa Cañarte.
Análisis formal: Escobar Paredes Rebeca Lucrecia, Solís Monar Lissette Gabriela, Pilar Asunción Soledispa Cañarte.
Investigación: Escobar Paredes Rebeca Lucrecia, Solís Monar Lissette Gabriela, Pilar Asunción Soledispa Cañarte.
Metodología: Escobar Paredes Rebeca Lucrecia, Solís Monar Lissette Gabriela, Pilar Asunción Soledispa Cañarte.
Administración del proyecto: Escobar Paredes Rebeca Lucrecia, Solís Monar Lissette Gabriela, Pilar Asunción Soledispa Cañarte.
Recursos: Escobar Paredes Rebeca Lucrecia, Solís Monar Lissette Gabriela, Pilar Asunción Soledispa Cañarte.
Software: Escobar Paredes Rebeca Lucrecia, Solís Monar Lissette Gabriela, Pilar Asunción Soledispa Cañarte.
Supervisión: Escobar Paredes Rebeca Lucrecia, Solís Monar Lissette Gabriela, Pilar Asunción Soledispa Cañarte.
Validación: Escobar Paredes Rebeca Lucrecia, Solís Monar Lissette Gabriela, Pilar Asunción Soledispa Cañarte.
Visualización: Escobar Paredes Rebeca Lucrecia, Solís Monar Lissette Gabriela, Pilar Asunción Soledispa Cañarte.
Redacción – borrador original: Escobar Paredes Rebeca Lucrecia, Solís Monar Lissette Gabriela, Pilar Asunción Soledispa Cañarte.
Redacción – revisión y edición: Escobar Paredes Rebeca Lucrecia, Solís Monar Lissette Gabriela, Pilar Asunción Soledispa Cañarte.