doi: 10.56294/hl2023224
ORIGINAL
Evaluation of the anti-inflammatory activity of the ethanol extract of higuerilla (Ricinus communis) leaves in wistar rats
Evaluación de la actividad antinflamatoria del extracto etanolico de hojas de higuerillas (Ricinus communis) en ratas wistar
Ariana Stefanía Dávila Moreno1, Emely Xiomara Quimi
Avilés1, Pilar Asunción Soledispa Cañarte1
![]()
1Universidad de Guayaquil, Facultad de Ciencias Químicas. Guayaquil, Ecuador.
Citar como: Dávila Moreno AS, Quimi Avilés EX, Soledispa Cañete PA. Evaluation of the anti-inflammatory activity of the ethanol extract of higuerilla (Ricinus communis) leaves in wistar rats. Health Leadership and Quality of Life. 2023; 2:224. https://doi.org/10.56294/hl2023224
Enviado: 24-04-2023 Revisado: 09-07-2023 Aceptado: 10-10-2023 Publicado: 11-10-2023
Editor: PhD.
Prof. Neela Satheesh ![]()
ABSTRACT
Currently, anti-inflammatory drugs are the most consumed worldwide, although their abuse and excess lead to gastropathies and cardiovascular complications causing death in 47 out of every 100 000 patients, Ricinus communis, despite its limited research, has proven to be an excellent natural alternative to counteract the inflammatory process. Therefore, the objective of this study is to evaluate the anti-inflammatory activity of the hydroalcoholic extract of higuerilla leaves by means of the plantar edema test with 3 % carregenin in mice, applied by cutaneous route inside the surface of the aponeurosis in the right paw, where five groups of treatments with six animals each were made; The first group was a negative control group with 0,9 % sodium chloride, the second group was a positive control group treated with indomethacin, while the other groups with the respective mixtures with a dose of 150, 250 and 500 mg/kg of hydroalcoholic extract of R. communis 50 % administered orally where they received an exact dosage according to weight and route of administration. Meanwhile, it was observed that the extract at the dose of 500 mg/kg. showed a similar behavior to Indomethacin at the maximum hour tested, with a similar percentage of inhibition after the second hour and over 50 % at the fourth hour of the study, which indicated a good anti-inflammatory power under the conditions. The extract at the other doses tested showed a good anti-inflammatory effect, although in lower percentages than the positive control. That is, it was found that under an effect of acute inflammation induced by significant plantar edema, it was presented with a higher percentage of inhibition at the dose of 500 mg/kg, comparable to indomethacin used as a reference drug.
Keywords: Inflammation; Anti-Inflammatory Effect; Total Polyphenols; Secondary Metabolites; Ricinus Communis.
RESUMEN
En la actualidad, los fármacos antiinflamatorios son los más consumidos mundialmente, a pesar de que su abuso y exceso conducen a gastropatías y complicaciones cardiovasculares causando la muerte en 47 de cada 100 000 pacientes, la Ricinus communis pese a su limitada investigación ha demostrado ser una excelente alternativa natural para contrarrestar el proceso inflamatorio. Por ello, el objetivo de este estudio es evaluar la actividad antiinflamatoria del extracto hidroalcohólico de hojas de higuerillas mediante el ensayo de edema plantar al 3 % de carregenina en ratones, aplicada por vía cutánea dentro de la superficie de la aponeurosis en la pata derecha, donde se confeccionó cinco grupos de tratamientos con seis animales cada uno; el primer grupo fue de control negativo con cloruro de sodio al 0,9 %, el segundo grupo de control positivo tratado con indometacina, mientras que los demás grupos con las mezclas respectivas con una dosis de 150, 250 y 500 mg/kg de extracto hidroalcohólico de R. communis al 50 % administrada por vía oral donde recibieron una dosificación exacta de acuerdo al peso y vía de administración. En tanto, se observó que el extracto a la dosis de 500 mg/kg manifestó un comportamiento similar a la Indometacina a la máxima hora ensayada, con un porcentaje de inhibición similar a partir de la segunda hora y superior al 50 % a la cuarta hora de estudio, lo que denotó un buen poder antiinflamatorio bajo las condiciones. El extracto a las otras dosis ensayadas demostró un buen efecto antiinflamatorio, aunque en porcentajes inferiores al control positivo. Es decir, se comprobó que bajo un efecto de inflamación aguda inducida por un edema plantar significativo, se presentó con un mayor porcentaje de inhibición a la dosis de 500 mg/kg, comparable a la indometacina usada como fármaco de referencia.
Palabras clave: Inflamación; Efecto Anti-Inflamatorio; Polifenoles Totales; Metabolitos Secundarios; Ricinus Communis.
INTRODUCCIÓN
Según el estudio de indicadores de prescripción racional de medicamento publicado por la Organización Panamericana de la Salud (PAHO) en la actualidad la correcta y adecuada administración de tratamientos farmacológicos en Latinoamérica es significativamente deficiente, en diversos cuadros clínicos de trastornos de salud agudos, cuadros de dolor e inflamación el diagnóstico médico y la prescripción de fármacos no se encuentra basada en evidencias puntuales, sino en estimaciones poco profesionales, en los que en su mayoría conlleva al uso y abuso de fármacos antinflamatorios, por lo que se estima que alrededor de 30 millones de pacientes utilizan a diario antiinflamatorios no esteroideos (AINE) en todo el mundo.(1,2,3,4,5,6,7,8)
Aunque los AINEs son la familia farmacológica con mayor consumo a nivel mundial, ya sea por prescripción médica o por automedicación, aun representa un alto riesgo de efectos secundarios adversos que conducen al desarrollo de patologías o intoxicaciones graves y/o crónicos debido a su uso inadecuado y abuso en su administración, siendo las principales patologías asociadas las hemorragias gastrointestinales, ulceraciones, perforaciones, cambios en la función renal, alteraciones cardiovasculares, daño hepatotóxico, etc..(9,10,11,12,13,14,15,16)
Además, de que en la población susceptible como los adultos mayores de 65 años en más del el 50 % se consideran inadecuados, puesto a que, puede ocasionar complicaciones severas, en especial, a aquellos con síndromes preexistentes como enfermedades cardiovasculares, enfermedades renales crónica, hipertensión, insuficiencia cardiaca y cirrosis. Por lo que, para evadir el abuso de estos medicamentos y sus posibles reacciones se ha difundido el empleo de “alternativas naturales” para el tratamiento de este tipo de síndromes inflamatorios.(17,18,19,20,21,22,23,24)
Desde la antigüedad se ha evidenciado el constante uso de especies vegetales para tratar o aliviar los síntomas de trastornos o síndromes patológicos debido a su bajo costo, accesibilidad y el reducido índice de toxicidad; que, en contraste con la actualidad y el consumo de fármacos sintéticos, aun es significativo convirtiéndose en la principal alternativa para la atención primaria de salud.
En especial, en poblaciones de estatus medio-bajo, en donde para sintomatologías frecuentes como inflamaciones leves o agudas, dolencias tolerables e incluso heridas de bajo riesgo son tratadas comúnmente con de brebajes y preparados de plantas con posibles propiedades farmacologías que se han popularizado mediante conocimientos ancestrales.(25,26,27,28,29,30,31,32)
Para el tratamiento de diversas patologías que involucran síndromes inflamatorios, dolores comunes y fiebre se han reconocido un sin número de especies vegetales con propiedades farmacológica antinflamatorias, analgésicas y antipiréticas, entre las que se encuentra la Ricinus communis L., que, aunque es una especie no comestible debido a que contiene compuestos tóxicos y alergénicos como la ricina y la ricinina, es ampliamente empleada tópicamente para tratar patologías como hemorroides, ictericia, úlcera, dolor de cabeza, llagas, epilepsia, reumatismo, y ciática.(33,34,35,36,37,38,39)
En Ecuador su cultivo y aprovechamiento no está intensamente desarrollado en contraste con otras especies como el cacao, o el banano, a pesar de su fácil manejo y resistencia a sequias, no obstante, existen campos dedicados a esta especie en las provincias de Santa Elena, Guayas y Manabí, aunque, su principal uso se encuentre orientado a la extracción del aceite de resino de sus semillas, el cual, es usado es a nivel industrial para producir lubricantes, o cosméticos.
Sin embargo, debido a la falta de respaldos científicos e información limitada acerca de su potencial farmacológico y mecanismo de acción preciso, su empleo en la en la industria farmacológica se ve comprometido, siendo utilizada con poca frecuencia en la aplicación medica profesional en el territorio ecuatoriano, a pesar de sus múltiples beneficios farmacológicos descritos en la medicina herbaria o etnomedicina trasmitida por generaciones en el país que incluyen el uso de los órganos de la especie como sus hojas y raíz como un potente antiinflamatorio y analgésico tópico, que hacen de esta especie un elixir de vida eficiente el tratamiento empírico de diversas patologías.(40,41,42,43,44,45,46,47)
Para contribuir al aprovechamiento farmacéutico de esta planta como una potencial fuente alternativa de biocompuestos activos de interés médico y comercial, se propuso el desarrollo del presente trabajo. En el primer capítulo, se presentan las bases de la problemática abordada y su justificación, además de la descripción de los objetivos y variables que se estudiaron y que guiaron la dirección de esta investigación.
En el segundo capítulo se encuentran las bases teóricas así como antecedentes en los cuales se fundamenta el estudio y conceptos asociados a la temática tratada; en el tercer capítulo se expone la metodología que se empleó para el desarrollo del presente estudio, seguido del cuarto capítulo donde se exhibe los resultados del mismo con los debidos argumentos y discusiones que se emitieron para resaltar la validez del mismo, finalizando con la sección de conclusiones, recomendaciones, referencia bibliográficas y anexos correspondientes al tema tratado.(48,49,50,51,52,53,54,55)
¿Cuál es el impacto potencial del extracto etanólico de hojas de higuerillas (Ricinus communis) en la actividad antiinflamatoria, evaluado en un modelo de ratas Wistar?
Objetivo
Evaluar la actividad antiinflamatoria en el extracto etanólico de las hojas de Higuerillas (Ricinus communis L) en ratas Wistar.
MÉTODO
Tipo de investigación
El tipo de investigación en el que se basa nuestro trabajo de investigación es de carácter cuantitativo y descriptivo, debido que este tipo de investigación, se manipulan deliberadamente las variables administrando diferentes concentraciones del extracto etanólico de hojas de higuerillas en ratas Wistar para evaluar su efecto antiinflamatorio. La investigación implica el control de las variables, la medición precisa de los resultados y la comparación de los grupos y de control.
El enfoque descriptivo y cuantitativo en cuanto a la medición de la respuesta antiinflamatoria en función de las concentraciones del extracto y la cuantificación de polifenoles totales Una de las variables dependientes empleadas en este estudio es el porcentaje de inflamación, y unas de las variables independientes empleadas son el extracto vegetal y las dosis empleadas en el experimento, evaluando el efecto antiinflamatorio esperado.

Figura 1. Flujograma de los procesos realizados del estudio
Equipos, Aparatos, Materiales y Reactivos
Equipos
· Balanza analítica
Aparatos
· Baño María
· Columna C18 5 µm x 4,6 mm × 250 mm
· Estufa programa a 90 ± 1 °C
· Mufla
· Reverbero calentador
Materiales
· Agitadores
· Tubos de ensayos
· Espátula
· Papel filtro
· Pipetas graduadas
· Pipetas Pasteur
· Pipetas volumétricas de 5, 10, 20, 50, 100 mL.
· Probeta
Reactivos
· Acetonitrilo
· Ácido clorhídrico 37 %;1 N.
· Ácido orto fosfórico 0,05 %
· Ácido sulfúrico concentrado
· Agua destilada
· Amoniaco
· Anhidrido
· acético glasear
· Cloroformo
· Cloruro de aluminio
· Cloruro férrico
· Etanol 96°
· Feling A y Feling B
· Formaldehido
· Hidróxido de Sodio 5 %; 20 %.
· Limadura de Magnesio
· Reactivo de Wagner
· Estufa programa a 90 ± 1 °C
· Mufla
· Reverbero calentador
· Pipetas volumétricas de 5, 10, 20, 50, 100 mL.
· Probeta
Muestra animal
Condiciones de tenencia de los animales
El modelo animal que se empleó en este ensayo fueron ratones de la línea CD-1, con peso corporal entre 25 y 30 g. El estudio se realizó en el Bioterio de la Facultad de Ciencias Químicas de la Universidad de Guayaquil.
Jaulas: Durante la climatización de los animales de experimentación fueron colocados en jaulas cómodas y seguras. Los bebederos y el sistema de distribución de alimentos fueron ubicados en contenedores de fácil acceso.
Agua y alimentación:A los animales se les proporcionó agua y alimentación ab libitum con las siguientes condiciones físicas: temperatura de 23 a 25 °C, humedad relativa 30-
70 % y fotoperiodo de luz de 12 a 12 semanas previas al desarrollo de la experimentación de los ratones que fueron adaptados a las condiciones del laboratorio.
Preparación del extracto:El extracto elaborado con la mezcla hidroalcohólica al 50 %, obtenido de las hojas de R. communis L. fue concentrado en un rotoevaporador a 40 oC hasta la total eliminación del etanol y se resuspendió en disolución de carboximetilcelulosa al 0,5 % (Sigma Aldrich).
Tamizaje Fitoquímico: Se refiere a la etapa preliminar de una investigación fitoquímica, sirve para identificar cualitativamente los principales metabolitos en una especie vegetal, guiando al investigador en siguientes fases de aislamiento y cuantificación de los grupos funcionales de interés.
Flavonoides – Ensayo de Shinoda
Prueba basada en la reacción del magnesio en medio acido, el cual es capaz de reducir el flavonoide presente en el extracto produciendo una coloración que varía de naranja a violeta cuya intensidad se da en función de la concentración de los flavonoides, además de generar un burbujeo.

Figura 2. Reacción química de la prueba de Shinoda

Figura 3. Procedimiento para identificación de flavonoides
Triterpenos – Ensayo de Liebermann-Burchard
Reacción que consiste en la adición de solución clorofórmica en un medio acido con anhídrido acético y una gota de ácido sulfúrico concentrado por la pared del tubo de ensayo generando la oxidación del triterpeno dando origen a una estructura con un doble enlace adicional, en donde en la primera etapa de la prueba el grupo OH del esterol se protona y pierde agua posteriormente, formándose el ion carbonio 3,5 colestadieno (74,68), que presente como una variación color de rosado a azul, o para después cambiar a verde intenso y visiblemente rápido si cambia a verde oscuro al finalizar la reacción, lo que indica la presencia de triterpenos y esteroides, recordando que diferenciar entre ambos metabolitos, los triterpenos se manifiestan por una coloración rosada, roja o purpura y los esteroles mediante pigmentaciones azul verdoso.
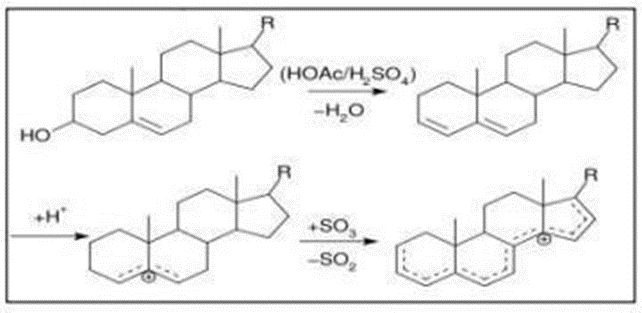
Figura 4. Reacción química de la prueba de Liebermann-Burchard
Figura 5. Reacción química de la prueba de Liebermann-Burchard
Saponinas – Ensayo de la espuma
Basada en la formación de espuma a partir del extracto vegetal, el cual es diluido con agua destilada, posteriormente se agita vigorosamente por un determinado periodo de tiempo, si esta alcanza una altura mínima de 2 mm y persiste durante más de 2 minutos el resultado es positivo.
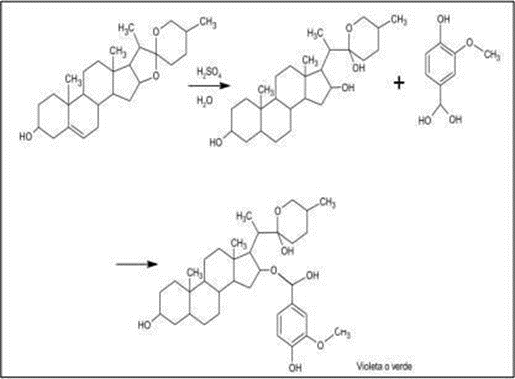
Figura 6. Reacción química de la prueba de formación de espuma

Figura 7. Procedimiento para identificación de saponinas
Quinonas – Reacción de Borntrӓnger
Consiste en la reacción que se generar entre el alcohol en un medio alcalino de NaOH al 5 o 10 %, y el extracto vegetal mediante agitación constante de la mezcla, que después se deja en reposo hasta observar una separación de fases debido a la producción de una hidrolisis de los ensalces glicosídicos de las quinonas y posterior oxidación de las antronas y antranoles hasta que los grupos antraquinónicos forman complejos de color rojos.
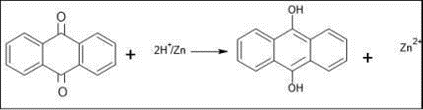
Figura 8. Reacción química de la Prueba de Borntrӓnger
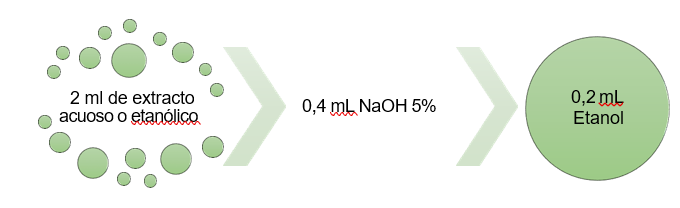
Figura 9. Procedimiento para identificación de quinonas
Mediante la formación de complejos fenólicos coloreados resultante de la adición de formaldehido en el extracto vegetal en conjunto con gotas de ácido clorhídrico concentrado, en baño maría se puede identificar dos tipos de taninos y compuestos fenólicos de manera que:
· Coloración rojo-vino: Presencia de compuestos fenólicos.
· Coloración verde intensa: Taninos del tipo pirocatecólicos.
· Coloración azul: Taninos del tipo pirogalotánicos.
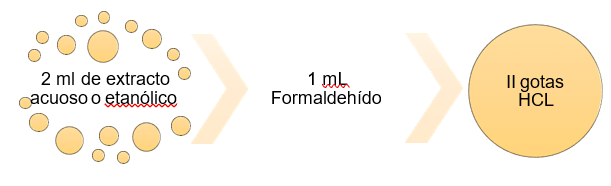
Figura 10. Procedimiento para identificación de taninos
Fenolatos Alcalinos y Betacianinas – Reacción con álcalis
Al interactuar el extracto vegetal con el hidróxido de sodio al 20 %, genera al reaccionar resultados positivos como:
· Fenolatos alcalinos: Decoloración lenta de violeta, azul, verde hasta amarillo.
· Betacianinas: Cambio rápido hasta el color amarillo.
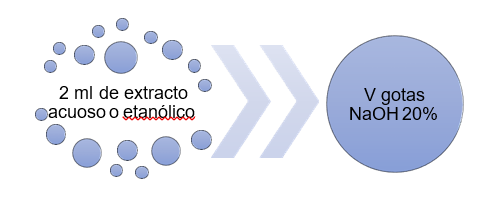
Figura 11. Procedimiento para identificación de Betacianinas y Fenolatos
Antocianinas – Reacción con amoniaco
· En el extracto obtenido al adicionarse amoniaco se produce una decoloración rápida desde violeta hasta amarillo, que demuestra la presencia de antocianinas.

Figura 12. Procedimiento para identificación de antocianinas
Betaleínas– Reacción con HCl
Los metabolitos presentes en el exacto reaccionan con el ácido clorhídrico formando dos resultados positivos:
· Antocianinas: Coloración rojo claro.
· Betaleínas: Pigmentación violeta oscuro.

Figura 13. Procedimiento para identificación de antocianinas y Betacianinas
Azúcares reductores - Ensayo de Fehling
El reactivo de Fehling formado de dos soluciones A compuesto por CuSO4 y B que contiene tartrato de sodio en NaOH reacciona con los azucares reductores (sacarosa, glucosa, fructosa), debido a que las aldosas y cetosas tiene la propiedad de oxidarse a sus respectivos ácidos carboxílicos, formando así el ácido glucónico. De forma que, el tartrato forma un complejo con el Cu+2 observándose una coloración azul en un resultado negativo, mientras que el resultado es positivo cuando el Cu+2 se reduce a Cu+ precipitándose como Cu2O, el cual se visualiza como un precipitado rojo ladrillo.
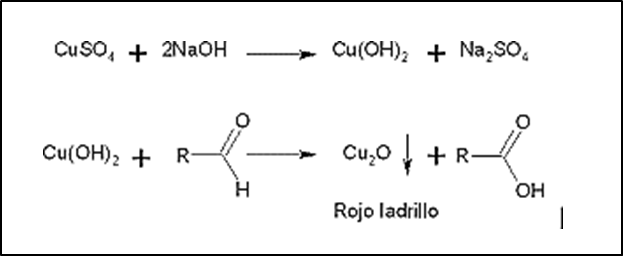
Figura 14. Reacción química del Ensayo de Fehling

Figura 15. Procedimiento para identificación de glucósidos Reductores
Alcaloides – Ensayo de Wagner
El reactivo de Wagner es una disolución alcohólica de I2/KI, que forma un complejo de triyoduro (I3-), debido a que el yodo (I2), actúa como un ácido frente al yoduro (I-). Este anión triyoduro presenta la capacidad de atraer electrostáticamente a alcaloides protonados, generando un complejo coloreado marrón rojizo, que indica un resultado positivo.
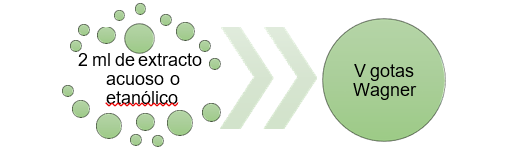
Figura 16. Procedimiento para identificación de Alcaloides
Cuantificación de Fenoles Totales por Folin-Ciocalteu
El ensayo Folin-Ciocalteu se emplea para determinar la concentración de los compuestos fenólicos totales en productos vegetales, basado en su reacción con el reactivo de Folin-Ciocalteu que es resulta de la mezcla de wolframato sódico y molibdato sódico en ácido fosfórico en pH básico que genera un cromógeno de coloración azul susceptible de ser determinada espectrofotométricamente a 765 nm.
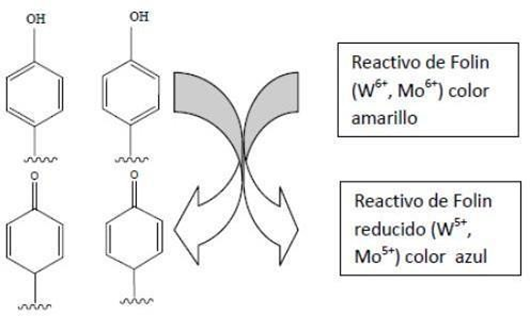
Figura 17. Reacción química del Ensayo de Folin-Ciocalteu
Puesto a que, el ácido fosfomolibdotúngstico resultante por las dos sales, al ser reducido por los grupos fenólicos da lugar a un complejo de color azul intenso, cuya intensidad es proporcional al contenido en polifenoles, por lo que resulta ser un método preciso y sensible, que puede padecer numerosas variaciones, fundamentalmente en lo relativo a los volúmenes utilizados de la muestra a analizar, concentración de reactivos y tiempo de reacción. Cabe resaltar para evitar inconvenientes debido a las variaciones e interferencias que se dan, aunque en raras ocasiones, se recomienda el uso del ácido gálico como patrón para compuestos fenólicos y quercetina para flavonoides.
Evaluación del Efecto Anti-inflamatorio
Se confeccionaron cinco grupos de tratamiento con seis animales cada uno según se muestra a continuación:
· Grupo I (control negativo): 0,3 mL de una disolución acuosa al 3 % de carragenina (agente inductor de la inflamación) en la aponeurosis plantar derecha y por la vía oral 10 mL/kg de solución de cloruro de sodio al 0,9 %.
· Grupo II (control positivo): 0,3 mL de una disolución acuosa al 3 % de carragenina (Sigma) en la aponeurosis plantar derecha y como agente antiinflamatorio Indometacina (Sigma Aldrich) 10 mg/kg por la vía oral.
· Grupo III (Ratones wistar): 0,3 mL de una disolución acuosa al 3 % de carragenina en la aponeurosis plantar derecha y mezcla hidroalcohólica de R. communis 150 mg/kg por la vía oral.
· Grupo IV (Ratones wistar): 0,3 mL de una disolución acuosa al 3 % de carragenina en la aponeurosis plantar derecha y mezcla hidroalcohólico de R. communis 250 mg/kg por la vía oral.
· Grupo V (Ratones wistar): 0,3 mL de una disolución acuosa al 3 % de carragenina en la aponeurosis plantar derecha y mezcla hidroalcohólico de R. communis 500 mg/kg por la vía oral.
Todos los animales recibieron una dosificación exacta de acuerdo al peso y la vía de administración utilizada. Inicialmente se midieron los volúmenes normales de la pata posterior derecha de los ratones con el uso de un pletismómetro digital (Panlab, España). Posteriormente, los compuestos de prueba fueron administrados por vía oral mediante el empleo de una cánula intragástrica. Transcurrido 30 minutos, se administró disolución acuosa de carragenina al 3 % en la aponeurosis plantar derecha de todos los animales. Los volúmenes de la pata inflamada se midieron a las 1, 2, 3 y 4 horas después de la administración de la carragenina. La diferencia entre el valor inicial y subsecuentes lecturas para cada tiempo de estudio arrojó el volumen de edema. Los porcentajes de inhibición de la inflamación se calcularon mediante la expresión siguiente.
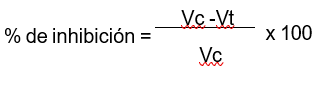
Donde:
Vc= valor medio del volumen de edema de los animales del grupo control negativo.
Vt= valor medio del volumen de edema de los animales del grupo tratado con la sustancia de prueba.
Al final del ensayo se procedió a sacrificar los animales empleando para ello una atmósfera saturada de éter, teniendo siempre en cuenta las técnicas de refinamiento planteadas actualmente para realizar los ensayos con animales de experimentación.
RESULTADOS
Tamizaje Fitoquímico del extracto hidroalcohólico
|
Tabla 1. tamizaje del extracto hidroalcohólico de Rinicus commnis L |
|||
|
Ensayos |
Observaciones |
Resulta dos |
Metabolitos |
|
Resinas |
Resinas |
- |
No precipitado |
|
Fehling |
Azúcares reductores |
++ |
Precipitado rojo ladrillo |
|
Baljet |
Lactonas/coumarinas |
++ |
Coloración roja |
|
Cloruro de hierro III |
Fenoles/ taninos |
++ |
Coloración verde – negro |
|
Espuma |
Saponinas |
++ |
Espuma de 1,5 cm por 1 hora |
|
Libermann- Burchard |
Triterpenos/esteroides |
+ |
Color verde |
|
Ninhidrina |
Aminoácidos/aminas |
± |
azul-violáceo |
|
Dragendorff |
Alcaloides |
- |
- |
|
Wagner |
Alcaloides |
- |
- |
|
Börntrager |
Quinonas |
- |
- |
|
Shinoda |
Flavonoides |
++ |
Fase amílica carmelita intensa |
|
Antocianidina |
Antocianidinas |
++ |
Color marron |
|
Kedde |
Cardiotónicos |
- |
Color verde oscuro |
|
Catequinas |
Catequinas |
- |
No cambia de color |
Determinación de fenoles totales y flavonoides totales
El contenido de fenoles totales fue determinado por el método de Folin-Ciocalteu, donde el reactivo, al reaccionar con los compuestos fenólicos presentes en una preparación, da lugar a un complejo de color azul que exhiben un máximo de absorción a 765 nm, lo cual permite su cuantificación por espectroscopia UV/visible y se expresan en equivalentes de ácido gálico.
En la cuantificación de flavonoides totales se utilizó el método colorimétrico del tricloruro de aluminio, donde dichos compuestos reaccionan con el reactivo, produciendo un complejo de color amarillo que posee un pico de absorción de luz a 415 nm.
En ambas cuantificaciones se lograron curvas de calibración con buena correlación entre las concentraciones ensayadas de las sustancias de referencias (ácido gálico y quercetina) y las absorbancias. El coeficiente de determinación (R2) fue ≥ 0,99, o sea, de 0,9988 y 0,9943 para fenoles y flavonoides, respectivamente; esto es indicativo del buen ajuste de la ecuación del modelo a los datos. En las figuras se ilustran las curvas de calibración de los patrones usados y se presentan los valores de fenoles y flavonoides.
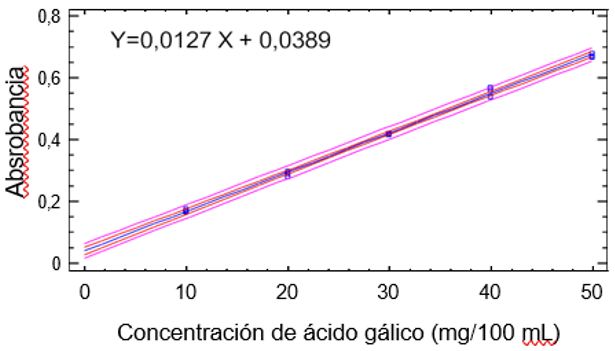
Figura 18. Curva de calibración del ácido gálico para la determinación de fenoles totales
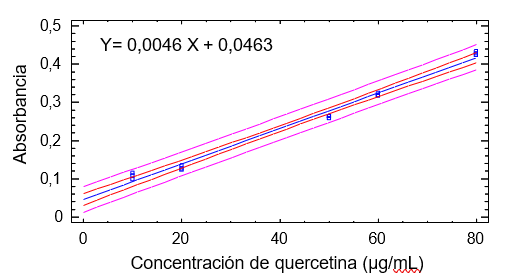
Figura 19. Curva de calibración de la quercetina para la determinación de flavonoides totales
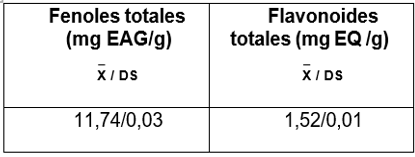
Figura 20. Contenido de fenoles totales y flavonoides totales en el extracto de R. communis
Evaluación del Efecto Antinflamatorio en ratas WISTAR
Consideraciones éticas
Todos los procedimientos y la manipulación de los animales, se realizaron siguiendo los principios éticos para el uso de los animales de laboratorio recomendados en los Lineamientos Internacionales.
Análisis estadístico
Los datos se expresaron como media aritmética/desviación estándar. Se empleó el análisis de varianza de una vía (ANOVA-1) para determinar si existía diferencia estadísticamente significativa para la variable evaluada y luego se aplicó la prueba post hoc de Tukey, para las comparaciones entre los grupos. Se trabajó a una significancia estadística de un valor de p<0,05 y un intervalo de confianza al 95 %. Los datos obtenidos en cada ensayo fueron procesados mediante el paquete estadístico SPSS para Windows versión 8.0.
RESULTADOS
Este método permite cuantificar de forma reproducible y sencilla dos de los parámetros más característicos de la inflamación como son el edema y la extravasación de plasma, al inducir una inflamación aguda localizada en la pata del animal tras la administración de carragenina en la aponeurosis plantar de la rata o ratón.
El modelo de edema inducido por carragenina en la pata de la rata o ratón es una prueba que se usa a menudo para investigar medicamentos antiinflamatorios, tanto esteroides como no esteroides, porque involucra numerosos mediadores. Es un método frecuente para probar los efectos antiedematosos de las sustancias naturales.
Una inyección subplantar de carragenina en la pata trasera provoca la inflamación en dos fases: la primera se desencadena por la histamina y la serotonina, mientras que la segunda, en la que el edema alcanza su punto máximo, se desencadena principalmente por la producción de prostaglandinas.
La Indometacina es utilizada con frecuencia como control positivo en este método, pues inhibe las ciclooxigenasas (COX) y por tanto, inhibe la formación y liberación de las prostaglandinas que en la segunda fase (entre las 3 y 4 horas) adquieren su máxima manifestación, principalmente la PGE2.
En la figura 20 se observa que a excepción del grupo control negativo cuyo volumen de edema fue aumentando en el tiempo, todos los grupos tratados mostraron los mayores valores de edema a la primera hora después de la administración de la carragenina. A partir de la segunda hora ocurre una disminución significativa en los volúmenes de edema hasta la cuarta hora que se obtiene el menor valor, lo que demuestra el efecto antiinflamatorio de la Indometacina y el extracto ensayado a las diferentes dosis.
Nótese como el menor valor de volumen de edema se percibe para la mayor dosis, o sea, se observa un efecto antiinflamatorio concentración dependiente. El extracto administrado a la dosis de 500 mg/kg de peso corporal tuvo un comportamiento comparable al fármaco de referencia, sin diferencias significativas en el transcurso del experimento.
|
Tabla 2. Volúmenes de edema durante las 5 horas de ensayo del control negativo, control positivo y extracto de R. comunis |
||||
|
Grupos |
Volumen de edema (mL) |
|||
|
1h |
2h |
3h |
4h |
|
|
NaCl 0,9 % |
0,171/0,00 6a |
0,175/0,00 5a |
0,183/0,00 5a |
0,188/0,00 6a |
|
Indometaci na |
0,151/0,00 3b |
0,121/0,00 3b |
0,111/0,00 3b |
0,087/0,00 2b |
|
Extracto 150 mg/kg |
0,153/0,00 6b |
0,144/0,00 5c |
0,123/0,00 6c |
0,121/0,00 7c |
|
Extracto 250 mg/kg |
0,154/0,00 5b |
0,132/0,00 6de |
0,120/0,00 3ce |
0,116/0,00 6c |
|
Extracto 500 mg/kg |
0,155/0,00 6b |
0,126/0,00 5be |
0,113/0,00 4be |
0,089/0,00 6b |
En la figura 21 se ilustran los porcentajes de inhibición de edema de los grupos sometidos al estudio. La Indometacina y el extracto a las diferentes dosis, fueron capaces de disminuir el edema producido por la carragenina en el transcurso de las cuatro horas. El extracto a la dosis de 500 mg/kg manifestó un comportamiento similar a la Indometacina a la máxima hora ensayada, con un porcentaje de inhibición similar a partir de la segunda hora y superior al 50 % a la cuarta hora de estudio, lo que denota un buen poder antiinflamatorio bajo las condiciones. El extracto a las otras dosis ensayadas también mostró un buen efecto antiinflamatorio, aunque con porcentajes inferiores al control positivo.

Figura 21. Porciento de inhibición del edema plantar en el tiempo del control positivo y el extracto de R. comunis
Ricinus communis L. es conocida como la planta de ricino. Es un arbusto oleaginoso perenne que pertenece a la familia Euphorbiaceae y subfamilia Acalyphoideae. La especie es originaria de África y actualmente se cultiva en muchas regiones tropicales y subtropicales de todo el mundo.
La especie posee propiedades como antiasmática, antidiabética, anticancerígena, antioxidante, antimicrobiana, efectos antiinflamatorios, antiulcerosos, cicatrizantes y laxantes. Se plantea que las hojas constituyen una fuente segura de agentes terapéuticos.
Como el modelo ensayado en la presente investigación se relaciona con la activación de mastocitos, liberación de cininas, mediadores como histamina, derivados del ácido araquidónico y especies de oxígeno reactivas, los extractos evaluados podrían contener moléculas con capacidad de modulación sobre dichos blancos.
Por otra parte, el efecto farmacológico señalado pudiera estar relacionado con determinados constituyentes químicos presentes en los extractos. Por ejemplo, se ha demostrado que taninos, flavonoides y saponinas son bien conocidas por su capacidad de inhibir la percepción del dolor y presentan propiedades antiinflamatorias debido a la inhibición de enzimas involucradas en la inflamación, especialmente, vía metabólica del ácido araquidónico y síntesis de prostaglandinas.
DISCUSIÓN
En la presente investigación se evaluó la actividad antiinflamatoria del extracto hidroalcohólico de hojas de Ricinus communis, sobre los primeros signos que aparecen durante la inflamación aguda (principalmente edema durante las primeras cuatro horas), mediante el ensayo de edema plantar por carragenina, el cual es mayormente utilizado en la actualidad para la evaluación de fármacos antiinflamatorios.(56,57,58,59,60,61,62)
A nivel global, las variantes pertenecientes al género analizado se emplean en la medicina tradicional debido a sus atributos antiinflamatorios, habiéndose documentado informes que respaldan esta aplicación. Sin embargo, hasta la fecha, no se ha investigado la viabilidad de utilizar la especie (Ricinus communis) con fines antiinflamatorios. Esta investigación representa el primer estudio in vivo, con un análisis histológico incluido.
Los flavonoides están presentes en cualquier parte del vegetal y tienen un importante papel en los procesos inflamatorios. Muchos son inhibidores de las cicloxigenasas, del óxido nítrico que es un mediador pleiotrópico de la inflamación. Otros inhiben el metabolismo del ácido araquidónico, por lo que evitan el incremento de prostaglandinas; en el ensayo de edema inducido por carragenina estos flavonoides han manifestado una elevada actividad antiinflamatoria.(63,64,65,66,67,68,69)
A diferencia de estas investigaciones previas, se preparó un extracto con mezcla hidroalcohólica al 50 % a partir de las hojas de R. communis que crece en Ecuador, no estudiada con anterioridad. Además, se utilizó como modelo ratones en lugar de ratas, brindando resultados promisorios como antiinflamatorios, corroborando lo anteriormente planteado para la especie de otras latitudes geográficas.(70,71,72,73,74,75,76)
Todas las dosis del extracto de planta y del fármaco estándar (Indometacina) mostraron un efecto inhibidor estadísticamente significativo (p < 0,05) sobre el aumento medio del volumen de la pata a partir de las 2 h en comparación con el grupo de control negativo. Se registró la inhibición mínima y máxima para todos los extractos y fármacos estándar 2 h y 4 h después de la administración de carragenina respectivamente.(77,78,79,80,81,82,83)
El efecto antiinflamatorio del extracto hidroalcohólico (al 70 %) de R. communis, a las dosis de 150, 250 y 500 mg/kg ha sido demostrado. Se observó actividad antiinflamatoria en el modelo de edema de oreja inducido por xileno, edema inducido por albúmina de huevo y carragenina en la pata de la rata, con porcentajes de inhibición superiores al 50 % a la máxima dosis ensayada.(84,85,86,87,88)
Otros estudios han demostrado el efecto antiinflamatorio in vitro del extracto hexánico, diclorometano, de acetato de etilo y metanólico de hojas en líneas celulares de macrófagos Raw 264.
Por su parte un estudio del efecto antiinflamatorio del extracto metanólico al 80 % a dos niveles de dosis (250 y 500 mg/kg) y fracciones de flavonoides totales en tres dosis diferentes (25, 50 y 100 mg/kg), en modelo agudo. Se demostró una potente acción antiinflamatoria a las mayores dosis evaluadas.
CONCLUSIONES
Con respecto al primer objetivo específico planteado, se logró la identificación del extracto etanólico mediante tamizaje fitoquímico de las hojas de Higuerillas (R. comunis L), donde dio positivo en el ensayo de Fehling con una precipitación de coloración rojo ladrillo, en el ensayo de Baljet con una precipitación de coloración roja, en el ensayo de Cloruro de hierro III con una coloración verde-negro, en el ensayo de espuma con una espuma de 1,5 cm por aproximadamente una hora, en el ensayo de Libermann-Burchard con una coloración verde, en el ensayo de Shinoda con una fase amílica carmelita intensa y en el ensayo de Antocianidina con una coloración marrón.
En cuanto a la cuantificación de la presencia de polifenoles totales en el extracto etanólico del Ricinus communis L por medio del método de Folin- Ciocalteu, se pudo determinar que en ambas cuantificaciones se lograron curvas de calibración con una buena correlación entre las concentraciones ensayadas de las sustancias de referencias y de las absorbancias, donde el coeficiente de determinación para fenoles fue 0,9988 y para flavonoides fue de 0,9943, lo cual es indicativo del buen ajuste de la ecuación del modelo a los datos.
En base al tercer objetivo específico planteado, se pudo determinar que el menor volumen de edema se percibe para la mayor concentración de la dosis, la cual fue una dosis de 500 mg/kg donde se obtuvo un comportamiento comparable al fármaco de referencia, en comparación a las otras dosis administradas donde se obtuvo un valor de inhibición mínima.
Por lo tanto, se concluye que la mezcla del extracto hidroalcohólico de R. communis mostró a todas las dosis ensayadas un efecto sobre la inflamación aguda al reducir el edema plantar significativamente, con mayor concentración de inhibición a la dosis de 500 mg/kg, comparable a la Indometacina usada como fármaco de referencia.
REFERENCIAS BIBLIOGRÁFICAS
1. Dorati R, Buschiazzo M, Marín A, Buschiazzo E, Rojas-Cortés R, Alfonso-Arvez J, et al. Indicadores de prescripción racional de medicamentos: factibilidad de aplicación en instituciones de las Américas. Pan Am J Public Health. 2021;45:1-11.
2. Silverio-Castellanos M, Silverio-Castellanos E, Santa Eulalia-Montoya R, Villa-Jiménez R. Cuba Salud: IV Convención Internacional de la Salud [Internet]. 2022 [cited 2022 Mar 5]. Available. https://convencionsalud.sld.cu/index.php/convencionsalud22/2022/paper/viewFile/218/1677.
3. Palacios-Montesdeoca DE, Miranda-Barros AA. Errores de prescripción en recetas médicas de antiinflamatorios no esteroideos en un centro de atención primaria de Ecuador. Soc Venezolana Farmacol Clín Terap. 2021;40(1):58-61.
4. Olry de Labry Lima A, Salamanca-Fernández E, Alegre del Rey EJ, Matas-Hoces A, González-Vera MA, Bermúdez-Tamayo C. Safety considerations during prescription of non-steroidal anti-inflammatory drugs (NSAIDs): A review of systematic reviews. An Sist Sanit Navar. 2022;44(2):261-73.
5. Linaris-Martínez DR. Efecto antiinflamatorio del extracto hidroalcohólico de las hojas de Luma chequen (Molina) A. Gray “Arayán” mediante el método de edema subplantar en ratas [thesis]. Lima: Universidad de Norbert Weiner; 2019.
6. Saini AK, Goyal R, Gauttam VK, Kalia AN. Evaluation of anti-inflammatory potential of Ricinus communis Linn leaves extracts and its flavonoids content in Wistar rats. J Chem Pharm Res. 2010;2(5):690-5.
7. Orlando-López W, Zambrano-Bazurto M, Zambrano-Gavilanes E. El cultivo de la higuerilla (Ricinus communis L.) y su situación actual en el Ecuador. Paideia XXI. 2022;12(2):373-90.
8. Maldonado-Santoyo M, Morales-López R. Análisis químico y nutricional en hojas de Ricinus communis. Rev Cubana Quím. 2022;34(1):1-18.
9. Prieto-Setién JM. Antiinflamatorios no esteroideos (AINES): ¿Dónde estamos y hacia dónde nos dirigimos? Cient Dent. 2007;4:203-12.
10. Yagüe-Sebastián MM, Coscollar-Escartín I, Muñoz-Albadalejo P, López-Canales MC, Villaverde-Royo MV, Gutiérrez-Moreno F. Use of topical non-steroidal anti-inflammatory agents in an urban health center: Comparison with current evidence. Med Fam SEMERGEN. 2013;39(6):304-8.
11. Saenz de Buruaga JA. Validez de la escalera analgésica de la OMS en reumatología. Semin Fundac Esp Reumatol. 2006;7(3):121-7.
12. Narvaes-Almeida EM, Verdugo-García JC. Análisis de la analgesia perioperatoria del paciente oncológico consumidor de opioides atendidos en el Hospital de Solca de Quito [thesis]. Quito: Pontificia Universidad Católica del Ecuador; 2019.
13. López-Castro R. Prevalencia del dolor en enfermos oncológicos: Dolor irruptivo. Med Paliat. 2015;22(1):2-9.
14. Coloma-Encalada KJ, Bobor-Tomalá GP. Evaluación de la actividad antiinflamatoria de la mezcla hidroalcohólica de Matricaria chamomilla y Urtica urens en ratas Wistar [thesis]. Guayaquil: Universidad de Guayaquil; 2015.
15. Duarte e Prato AA. Reacciones de hipersensibilidad a los antiinflamatorios no esteroideos [thesis]. Murcia: Universidad de Murcia; 2010.
16. González Costa M, González Alexander A. La inflamación desde una perspectiva inmunológica: Desafío de la medicina. Rev Haban Cienc Méd. 2019;18(4):30-44.
17. Sánchez-Serrano J, Tenias-Burillo M, Chinchilla-Fernández C, Jiménez-López A, Padilla-Serrano F, Calleja-Hernández MA. Asociación entre el síndrome coronario agudo y el consumo de antiinflamatorios no esteroideos. Rev Cient Ars Pharm. 2015;56(1):1-7.
18. Organización Mundial de la Salud. Perspectivas políticas sobre medicamentos de la OMS: Promoción del uso racional de medicamentos: Componentes centrales. Ginebra: OMS; 2002.
19. Bravo-Bravo KJ, Espinel-Martínez DE, Pardo-Arias PA, Robles-Duarte A. Automedicación en estudiantes de medicina de la Universidad de Ciencias Aplicadas y Ambientales U.D.C.A en el segundo semestre de 2017 [thesis]. Bogotá: U.D.C.A.; 2017.
20. Fajardo-Zapata AL, Méndez-Casallas FJ, Hernández-Niño JF, Molina LH, Tarazona M, Nossa LM, et al. La automedicación de antibióticos: Un problema de salud pública. Salud Barranquilla. 2013;29(2).
21. Castro-Cataño E, Pechené-Paz E, Rocha-Tenorio C, Loaiza-Buitrago P. Automedicación en estudiantes de pregrado de enfermería. Enferm Glob. 2022;21(66).
22. Tobón-Marulanda FA, Montoya-Pavas S, Orrego-Rodríguez MA. Family self-medication: A public health problem. Educ Méd. 2018;19:122-7.
23. Romero-Bedoya CE. Administración de fármacos sin prescripción médica a pacientes pediátricos que acuden a emergencias en el hospital Pablo Arturo Suárez [thesis]. Quito: Universidad Pontificia Católica del Ecuador; 2018.
24. Moreno-Royo L, Muedra-Navarro V. Bases del dolor: Farmacología básica del dolor (analgésicos). In: Máster en Abordaje Integral del Dolor. Madrid: Editorial Médica Panamericana; 2022. p. 1-15.
25. García-Barrero P. Inflamación. IX Programa de Promoción de la Cultura Científica y Tecnológica. 2008;102(1).
26. Administración Nacional de Medicamentos, Alimentos y Tecnología Médica; Instituto Nacional de Medicamentos. Farmacopea Argentina [Internet]. 2013 [cited 2022 Mar 5]. Available from: https://www.argentina.gob.ar/sites/default/files/farmacopea_argentina_2013_ed.7.pdf.
27. Díaz-Velastegui A, Reyes De la Cruz SJ. Estudio bibliográfico preclínico comparativo del efecto normoglucemiante de extractos de Azadirachta indica (neem) y Murraya koenigii (curry) [thesis]. Guayaquil: Universidad de Guayaquil, Facultad de Ciencias Químicas; 2022.
28. Santamaría C, Martín-Gonzáles A, Astorga F. Extractos vegetales: Aplicación para la reducción del estrés [Internet]. 2015 [cited 2022 May 5]. Available from: https://nutricionanimal.info/download/0315-ena-WEB.pdf.
29. Castillo-España P, Perea-Arango I, Arellano-García JdJ, Valencia-Díaz S. ¿Qué son y para qué sirven los metabolitos de las plantas? [Internet]. 2019 [cited 2022 May 21]. Available from: https://www.cyd.conacyt.gob.mx/?p=articulo&id=227.
30. Purkayasthaa J, Nath SC, Islam M. Ethnobotany of medicinal plants from Dibru-Saikhowa Biosphere Reserve of Northeast India. Fitoterapia. 2005;76(1):121-7.
31. Singh PP, ACSMS. Activity-guided isolation of antioxidants from the leaves of Ricinus communis L. Food Chem. 2009;114(3):1211-5.
32. Anil KS, Rohit G, Vinod KG, Adjudhia NK. Evaluation of anti-inflammatory potential of Ricinus communis Linn leaves extracts and its flavonoids content in Wistar rats. J Chem Pharm Res. 2010;2(5):690-5.
33. Perez J. Estudio fitoquímico y actividad antiinflamatoria del extracto hidroalcohólico de las hojas de Ricinus communis L. “Higuerilla” [thesis]. Lima: Universidad Nacional Mayor de San Marcos; 2013.
34. Hussain A, Aslam N, Muhammad N, Muhammad Naeem. In vitro antioxidant activity and in vivo anti-inflammatory effect of Ricinus communis (L.) and Withania somnifera (L.) hydroalcoholic extracts in rats. Hum Anim Health. 2021;64.
35. Dolores BMR. Screening fitoquímico y evaluación de la actividad antimicrobiana de Catharanthus roseus (L.) G. Don, Justicia pectoralis Jacq. y Scoparia dulcis L. FIGEMPA Investig Desarroll. 2017;1(2).
36. Nemudzivhadi V, Masoko P. Evaluación in vitro de la citotoxicidad, actividades antioxidantes y antiinflamatorias de los extractos de hojas de Ricinus communis (Euphorbiaceae). Evid Based Complement Alternat Med. 2014;2014:8.
37. Ilavarasan R, Mallika M, Venkataraman S. Actividad antiinflamatoria y eliminadora de radicales libres del extracto de raíz de Ricinus communis. Ethnopharmacol Commun. 2006;103(3):485-91.
38. Lomash V, Parihar SK, Jainista NK, Katiyar AK. Efecto de los extractos de Solanum nigrum y Ricinus communis sobre la inflamación inducida por histamina y carragenina en la piel de pollo. Gen Doc. 2015;56.
39. Chouhan HS, Jain G. Medicinal properties of Ricinus communis: A review. Int J Pharm Sci Res. 2021;12(7)..
40. Peña-Urbe DJ. Morfometría y fisiología de plantas de ecotipos silvestres de higuerilla (Ricinus communis L.) del norte de México [doctoral thesis]. Bermejillo: Universidad Autónoma Chapingo; 2021.
41. Jena J, Gupta A. Ricinus communis Linn: Una revisión fitofarmacológica. Int J Pharm Pharm Sci. 2012;4(4):25-9.
42. Thompson MJ, Bowers WS. Lupeol y 30-norlupan-3β-ol-20-one del recubrimiento de la semilla de ricino (Ricinus communis L.). Phytochemistry. 1968;7(5):845-7.
43. Sen SK, Behera LM. Usos etnomedicinales de algunas plantas para curar heridas del distrito de Bargarh en el oeste de Odisha, India. Int J Herb Med. 2021;9(2):14-7.
44. Kumar M. Una revisión de los constituyentes fitoquímicos y las actividades farmacológicas de Ricinus communis L. Int J Pharmacogn Phytochem Res. 2017;9(4):466-7.
45. Majumder M, Debnath S, Gajbhiye RL, Saikia R, Gogoi B, Samanta SK, et al. El extracto de frutas de Ricinus communis L. inhibe la migración/invasión, induce apoptosis en células de cáncer de mama y detiene la progresión del tumor in vivo. Sci Rep. 2019;9(1):1-4.
46. Paz-Naranjo J, Gómez de Saravia S, Battiston P, Larionova M, Guiamet P. Fracción aislada de Ricinus communis L. (Euphorbiaceae) en el control del biodeterioro de documentos patrimoniales. Dominguezia. 2015;3(2):24-9.
47. Escoto-García T, Rutiaga-Quiñones JG, Orihuela-Equihua A. Estudio químico, micrográfico y morfológico de Ricinus communis L., y su aplicación en pulpa blanqueable. Conciencia Tecnol. 2014;48:1-6.
48. Rivera-Vicuña DW. Actividad antiinflamatoria del extracto etanólico de las hojas de Baccharis buxifolia (Lam.) Pers. “Talla” en ratones [thesis]. Lima: Escuela Académico Profesional de Farmacia y Bioquímica, Facultad de Farmacia y Bioquímica; 2018.
49. Saquicela A, Pérez-Ramírez JE, Díaz-Piedrahita MA, Caichug-Rivera DM, Santillán-Lima JC, editors. Suturando conocimientos en el arte de la cirugía. 1st ed. La Plata: Puerto Madero Editorial Académica; 2022.
50. Bordes-Gonzales F. Fases de la inflamación [Internet]. 2010 [cited 2023 Jun 13]. Available from: https://ruidera.uclm.es/xmlui/bitstream/handle/10578/266/1994-5.pdf.
51. Mendez-Jesus IR. Fases de la inflamación [Internet]. 2019 [cited 2023 Jun 15]. Available from: https://www.studocu.com/ec/document/universidad-tecnica-de-cotopaxi/biologia-molecular/fases-de-la-inflamacion/12231851.
52. Borges AA, León-Regal ML, De Armas-García JO, Miranda-Alvarado L, Varens-Cedeño JA, Cuesta del Sol JÁ. Respuesta inflamatoria aguda: Consideraciones bioquímicas y celulares. Rev Finlay. 2015;5(1):1-5.
53. Leal M. Evaluación del efecto antiinflamatorio de un concentrado de frutos de Aristotelia chilensis en un modelo de inflamación aguda subplantar inducida por carragenina en ratas [thesis]. Valdivia: Universidad Austral de Chile, Escuela de Medicina Veterinaria; 2009.
54. Divins MJ. Antiinflamatorio. Farm Prof. 2014;28(5):1-5.
55. Espinós-Pérez D, López-Buendicha A, Calvo ME. Bases farmacológicas y tratamiento de la inflamación. Informe. Real Academia Nacional de Farmacia; 2009.
56. Rivera-Ordónez A. AINES: Su mecanismo de acción en el sistema nervioso central. Rev Mex Anestesiol. 2006;29(1):1-4.
57. Perea-Martínez A, López-Navarrete G, De la Osa-Busto M, Reyes-Gómez U. Antiinflamatorios no esteroideos y sus aplicaciones terapéuticas. Bol Clín Hosp Infant Edo Son. 2016;33(2):1-5.
58. M. L. Analgésico, antipirético y antiinflamatorios no esteroideos (AINES). Lima: Universidad Cayetano Heredia, Facultad de Estomatología; 2003.
59. Palomino-Ayme MA. Actividad antiinflamatoria del extracto hidroalcohólico del botón floral de Syzygium aromaticum (L.) Merr. G. L. M., Perry. “Clavo de Olor” [thesis]. Ayacucho: Escuela de Formación Profesional de Farmacia y Bioquímica, Facultad de Ciencias Biológicas; 2014.
60. García-Rodriguez LA, Hernandez-Díaz S. The risk of upper gastrointestinal complications associated with nonsteroidal anti-inflammatory drugs, glucocorticoids, acetaminophen and combinations of these agents. Arthritis Res. 2001;3:98-101.
61. Watkins PB, Slattery JT, Kaplowitz N, Colonese CR, Colucci SV, Stewart PW, et al. Aminotransferase elevations in healthy adults receiving 4 grams of acetaminophen daily: A randomized controlled trial. JAMA. 2006;296:87-93.
62. Kearney PM, Baigent C, Godwin J, Halls H, Emberson JR. Do selective cyclooxygenase-2 inhibitors and traditional non-steroidal anti-inflammatory drugs increase the risk of atherothrombosis? Meta-analysis of randomized trials. BMJ. 2006;332:1302-8.
63. Curhan GC, Willett WC, Rosner B, Stampfer MJ. Frequency of analgesic use and risk of hypertension in younger women. Arch Intern Med. 2002;162:2204-8.
64. Forman JP, Rimm EB, Curhan GC. Frequency of analgesic use and risk of hypertension among men. Arch Intern Med. 2007;167:394-9.
65. Massey T, Derry S, Moore RA, McQuay HJ. Topical NSAIDs for acute pain in adults. Cochrane Database Syst Rev. 2010;2010(6):CD007402.
66. Moore RA, Derry S, McQuay HJ. Topical agents in the treatment of rheumatic pain. Rheum Dis Clin North Am. 2008;24:415-32.
67. Serra HA, Roganovich JM, Rizzo LF. Glucocorticoides: Paradigma de medicina traslacional de lo molecular al uso clínico. Medicina (B Aires). 2012;72:1-10.
68. Baños-Falcones JD, Fajardo-Parrales GG. Análisis del perfil fitoquímico de semillas y estudio preclínico bibliográfico del efecto normoglucemiante de extractos acuosos y etanólicos (Syzygium malaccense) [thesis]. Guayaquil: Universidad de Guayaquil, Facultad de Ciencias Químicas; 2022.
69. Instituto Químico Biológico. Principios de la farmacología: Principios de la toxicología [Internet]. 2004 [cited 2022 Jul 5]. Available from: https://www.iqb.es/cbasicas/farma/farma05/tox/tox02.htm.
70. García-García E. Dosificación farmacológica: Cálculo de dosis. SalusPlay; 2017.
71. Estrada-Campmany M. Dosificación y márgenes terapéuticos. Offarm. 2006;25(5):1-5.
72. Arias D. Glosario de medicamentos, desarrollo, evaluación y uso. León-Tapia J, editor. Washington, D.C.: Organización Panamericana de la Salud; 1999.
73. Universidad de Valencia. Métodos de evaluación in vivo/in vitro de fármacos antiinflamatorios, antialérgicos e inmunosupresores [Internet]. 2012 [cited 2022 Jul 5]. Available from: https://www.uv.es/biomefar/Guias_docentes_2013/Metodos%20de%20evaluacion%20in%20vivo-invitro%20de%20farmacos.pdf.
74. Cabrera JS. Identificación primaria de metabolitos secundarios de Ulex europaeus L. “retamo espinoso” y su actividad biológica [thesis]. Bogotá: Universidad de la Salle, Departamento de Ciencias Básicas; 2020.
75. García AP, Tamargo B, Salas E, Calzadilla C, Acevedo R, Sierra G. Tamizaje fitoquímico de extractos obtenidos de la planta Sapindus saponaria L. que crece en Cuba. Rev Bionatura. 2020;5(3):1-10.
76. Ramos ACC. Análisis fitoquímico, determinación cualitativa y cuantitativa de flavonoides y taninos, actividad antioxidante, antimicrobiana de las hojas de Muehlenbeckia hastulata (J.E.Sm) I.M. Johnst de la zona de Yucay (Cusco) [thesis]. Lima: Universidad Nacional Mayor de San Marcos, Facultad de Química e Ingeniería Química; 2016.
77. Castillo OV. Estudio de sustancias naturales como indicadores de pH: Una propuesta didáctica. An Quím. 2020;116(2):1-8.
78. Padilla AGO. Estudio comparativo del rendimiento y contenido de grado alcohólico por fermentación controlada con levaduras en agua miel de penco [thesis]. Cuenca: Universidad del Azuay, Ingeniería en Alimentos; 2017.
79. Granados RUG, Cruz-Sosa F, Alarcón-Águila FJ, Nieto-Trujillo A, Martínez MEG. Análisis fitoquímico cualitativo de los extractos acuosos de Thalassia testudinum Banks ex König et Sims de la localidad de Champotón, Campeche, México, durante el ciclo anual 2016-2017. Polibotánica. 2019;48:1-15.
80. García-Martínez E, Fernández-Segovia I, Fuentes-López A. Métodos de evaluación y resultados en química de alimentos [Internet]. Valencia: ETSIAMN, Universitat Politècnica de València; 2015. Available from: https:/
81. Velázquez AP. Introducción a la farmacología [thesis]. La Habana: Universidad de Ciencias Médicas de La Habana, Facultad de Ciencias Médicas; 2016.
82. Murillo MC. Ratas, ratones, conejos… ¿Qué son biomodelos y para qué se usan? Rev Biol Trop. 2018;2(1):1-5.
83. Ize I, Zuk M. La evaluación dosis-respuesta al evaluar el riesgo de la salud humana [Internet]. 2010 [cited 2022 Mar 13]. Available from: http://www2.inecc.gob.mx/publicaciones2/libros/636/dosis.pdf.
84. Hernández-Chávez A. Farmacología general: Una guía de estudio. 1st ed. México: McGraw-Hill Interamericana Editores, S.A. de C.V.; 2014.
85. Martínez-Taveras F. Fitoquímica y etnofarmacología: Definición de conceptos y aplicación a la carrera de Química y Farmacia de la Universidad de La Frontera [master’s thesis]. Temuco, Región de La Araucanía, Chile: Universidad de La Frontera; 2020.
86. López RSB, Vélez JPA. Análisis de fitoesteroles en la semilla de Persea americana Miller (Var. Lorena) por cromatografía de gases y cromatografía líquida de alta eficiencia. Rev Fac Cienc Básicas. 2017;13(1):1-10.
87. Gupta E. Innovations in food technology. In: β-Sitosterol: Predominant phytosterol of therapeutic potential. Uttar Pradesh: Springer Nature Singapore; 2020. p. 465-77.
88. Mendoza-Urrutia L, Salvatierra-Laytén FV. Perfil del consumidor de antiinflamatorios no esteroideos en Chiclayo y Cajamarca. Acta Méd. 2008;19(3):216-9.
FINANCIACIÓN
Ninguna.
CONFLICTO DE INTERÉS
Los autores declaran que no existe conflicto de interés.
CONTRIBUCIÓN DE AUTORÍA
Conceptualización: Ariana Stefania Dávila Moreno, Emely Xiomara Quimi Avilés, Pilar Asunción Soledispa Cañete.
Curación de datos: Ariana Stefania Dávila Moreno, Emely Xiomara Quimi Avilés, Pilar Asunción Soledispa Cañete.
Redacción – borrador original: Ariana Stefania Dávila Moreno, Emely Xiomara Quimi Avilés, Pilar Asunción Soledispa Cañete.
Redacción – revisión y edición: Ariana Stefania Dávila Moreno, Emely Xiomara Quimi Avilés, Pilar Asunción Soledispa Cañete.